Иммунологический анализ крови
О том, какие бывают анализы крови с точки зрения иммунологической системы человека, мало кто знает, так эти анализы не так распространены. Как правило, такое исследование крови дает информацию о вирусе иммунодефицита в организме человека и является анонимной, так как проводится по желанию пациента. Для забора используют взятую натощак из вены кровь, из которой для исследования методом центрифугирования получают сыворотку. Кроме этого, изучение сыворотки крови способно выявить ряд венерических заболеваний (сифилис, герпес, хламидиоз), а также все виды гепатита, корь, краснуху, паротит и токсоплазмоз.
В основном, для проведения ИФА анализа, исследуемым биологическим материалом является кровь, однако, исследованию может подвергаться спинномозговая жидкость, содержимое стекловидного тела, околоплодные воды и др.
Что такое иммуноглобулин (антитело)?
Иммуноглобулины – это иммунные молекулы, способные связываться и нейтрализовать большинство инфекционных возбудителей и токсинов в организме. При этом важнейшей характеристикой иммуноглобулинов является их специфичность, то есть способность связываться с определенным антигеном. Именно это свойство используется для проведения анализа крови на иммуноглобулин.
Существует пять типов иммуноглобулинов, однако наиболее изученными являются иммуноглобулины А, М, и G. Иммуноглобулины М и G проявляют свою активность в крови. Иммуноглобулины А являются, своего рода, барьером на поверхности слизистых оболочек, так как присутствуют там в большом количестве.
Иммунологический анализ крови позволяет определять тип иммуноглобулинов, благодаря этому ИФА позволяет не только диагностировать заболевание, но и определить стадию данного и отслеживать динамику заболевания:
- В первые 2 недели заболевания обнаруживаются только иммуноглобулины А.
- Со 2-й по 3-ю неделю заболевания в крови обнаруживаются иммуноглобулины А и М.
- С 3 по 4 неделю анализ крови на иммуноглобулин определяются все три типа.
- При выздоровлении в крови пропадают иммуноглобулины М, а количество А и G снижается в 2 – 4 раза.
- При наличии хронического процесса в крови обязательно присутствуют иммуноглобулины G, иммуноглобулины М отсутствуют, иммуноглобулины А могут как присутствовать, так и отсутствовать.
Достоинства иммуноферментного анализа (ИФА):
- Относительно высокая чувствительность (точность).
- Приемлемая стоимость.
- Позволяет проводить раннюю диагностику (благодаря возможности определения классов иммуноглобулинов при анализе).
- Позволяет отслеживать динамику инфекционного процесса (благодаря возможности определения классов иммуноглобулинов).
- Удобство в работе.
- Иммунологический анализ крови позволяет получить быстрый ответ.
Недостатки ИФА анализа крови:
Иногда иммуноферментный анализ дает ложноположительные или ложноотрицательные результаты.
Область применения иммунологического анализа крови
- Диагностика вирусных заболеваний: гепатиты, герпес, Эпштейн-Барр вирус, цитомегаловирус и др.
- Инфекции передающиеся половым путем: хламидиоз, гонорея, трихомонада, микоплазма, уреаплазма.
- Сифилис.
- Эндокринология (определение уровня гормонов).
- Онкомаркеры (диагностика онкологических заболеваний).
- Иммунология (диагностика иммунодефицита).
- Аллергология (диагностика и лечение аллергий).
Серологический анализ крови – лабораторный метод исследования крови, который применяется с целью диагностики инфекционных заболеваний и определения стадии инфекционного процесса. Серологическая реакция основана на взаимодействии антител и антигенов.
Определение антигенов используют для определения родовой и видовой принадлежности микроорганизмов. Данный метод исследования применяется в урологии и венерологии. Кровь для серологического анализа крови берется утром натощак из вены.
Осложнения
Наиболее частые — сепсис (нередко стафилококковый), прободение кишечника (чаще подвздошной кишки, так как она более чувствительна к цитостатическому воздействию), медиастинит, пневмонии, нома; реже — тяжелый отек слизистой оболочки кишки с образованием непроходимости, перитонита. Серьезным осложнением является острый эпителиальный гепатит, который часто развивается уже после ликвидации АГРАНУЛОЦИТОЗА. Отсутствие гранулоцитов придает своеобразие течению инфекционных осложнений — отсутствие гнойников, преобладание некрозов. Пневмонии протекают на фоне скудных физикальных данных: притупление едва заметно, хрипов, выраженного бронхиального дыхания может не быть, выслушивается лишь крепитация над областью поражения. Рентгенологические изменения очень скудные.
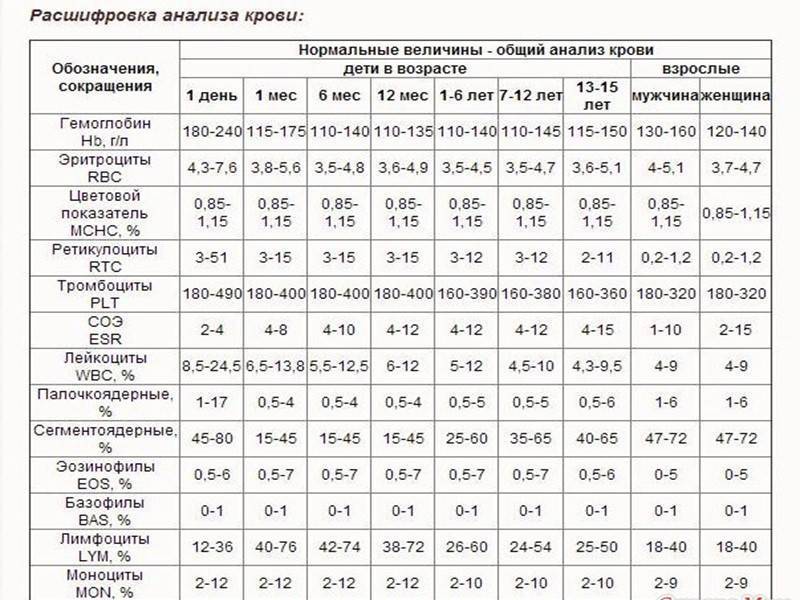
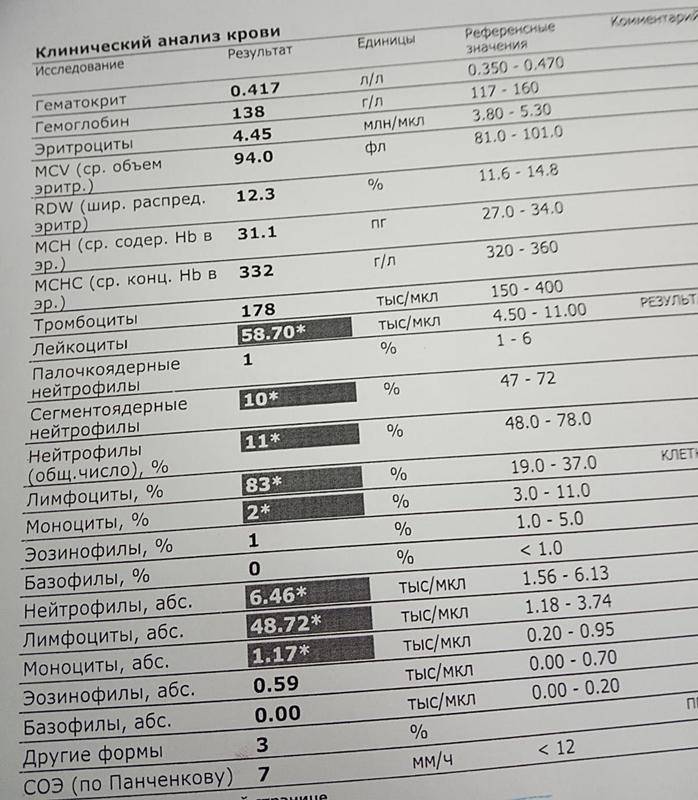
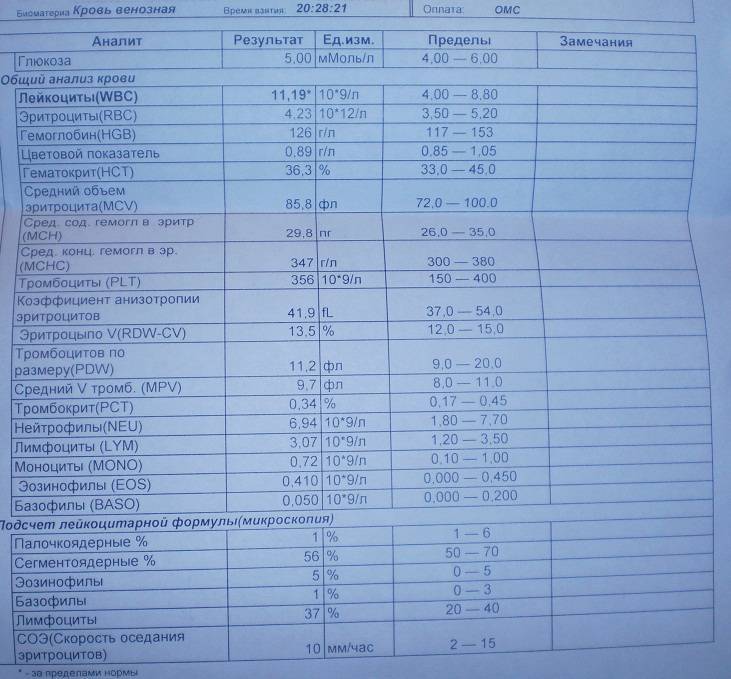
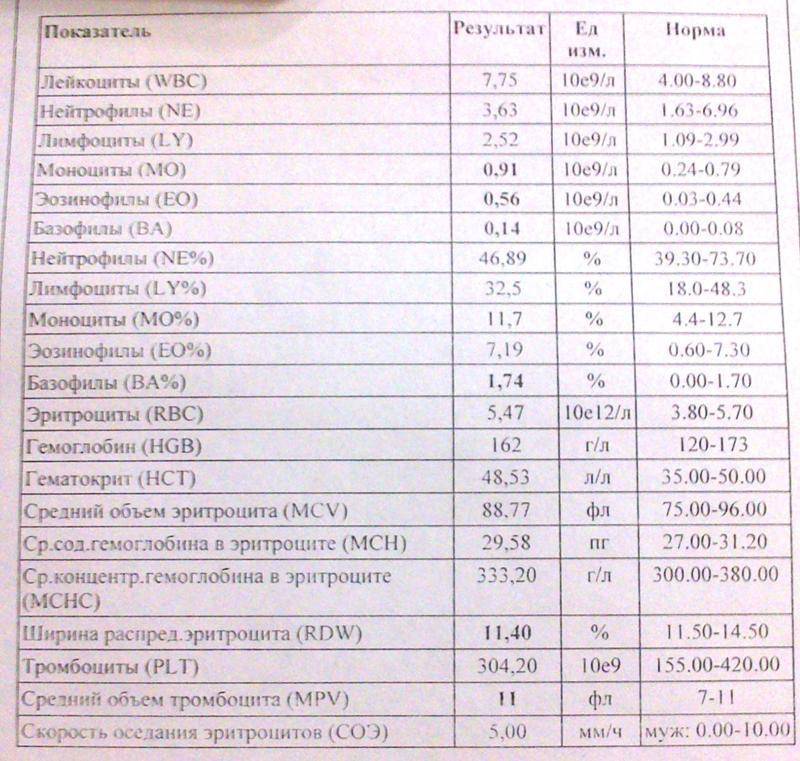
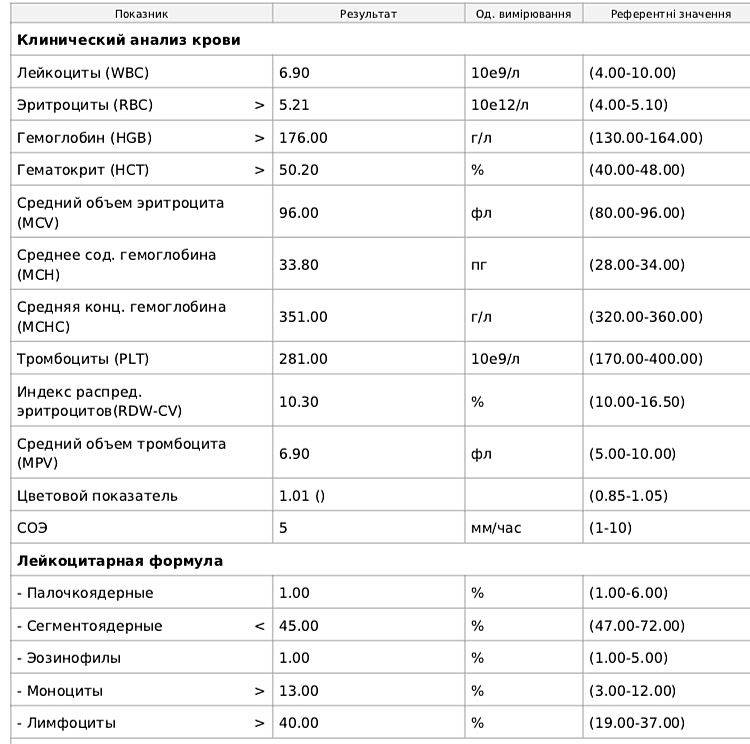
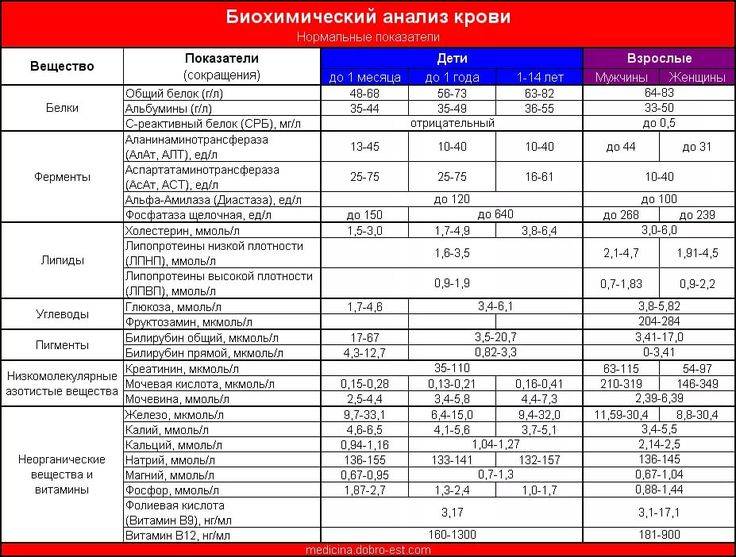
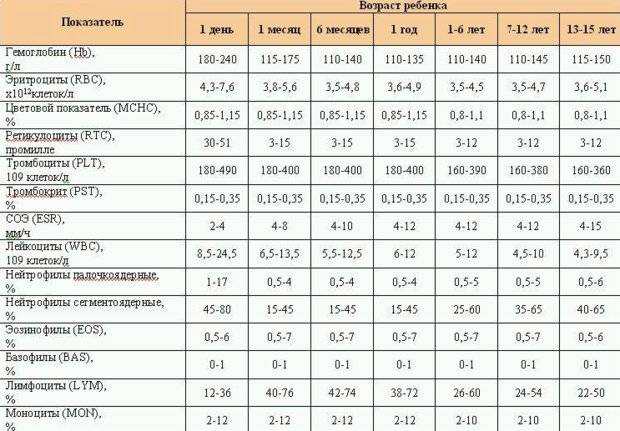
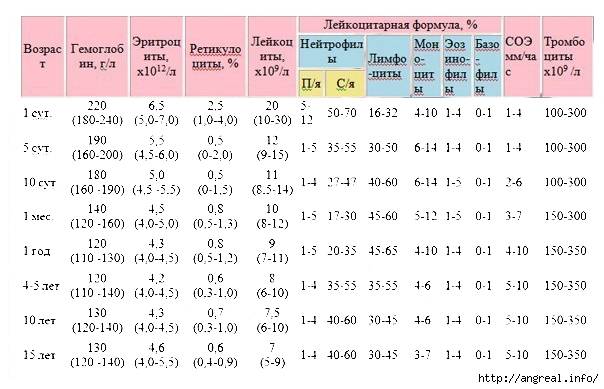
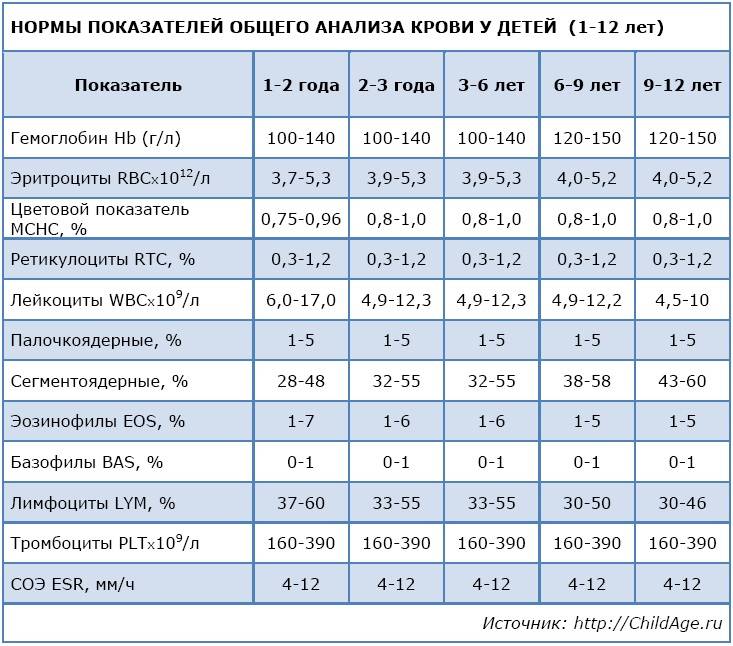
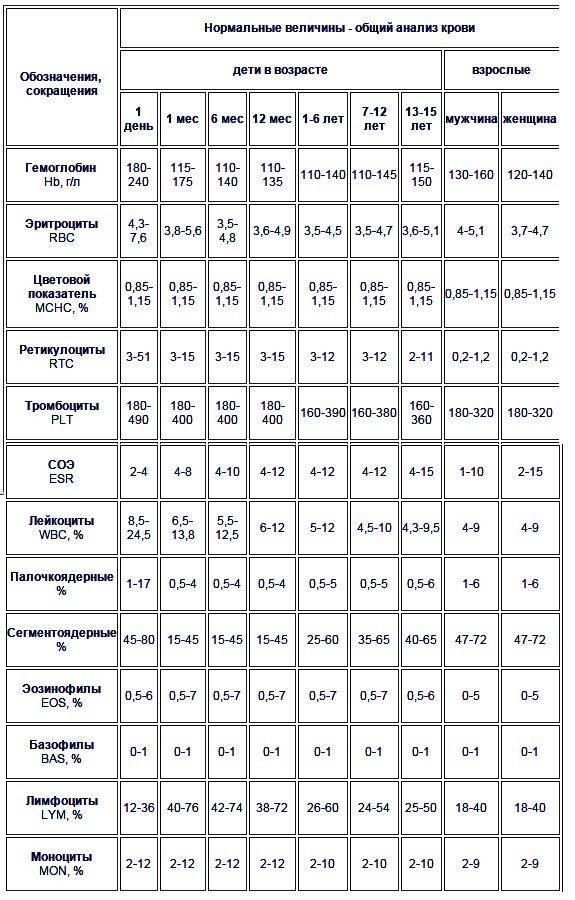
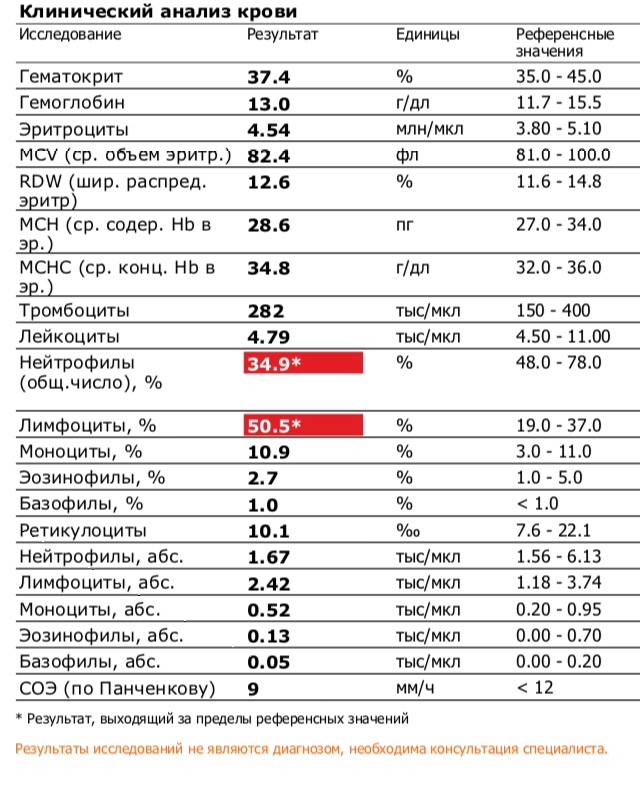
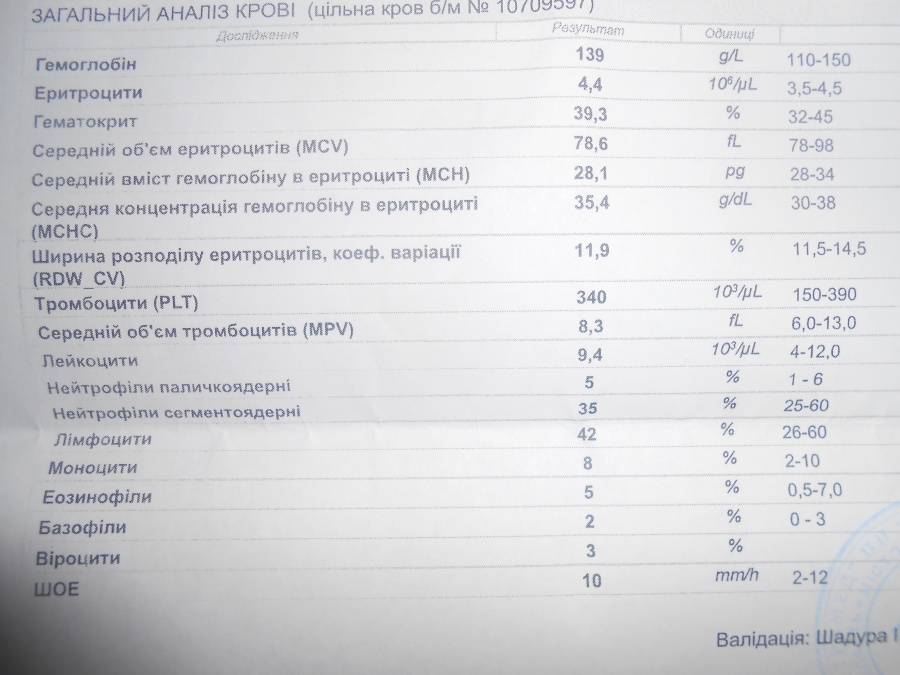
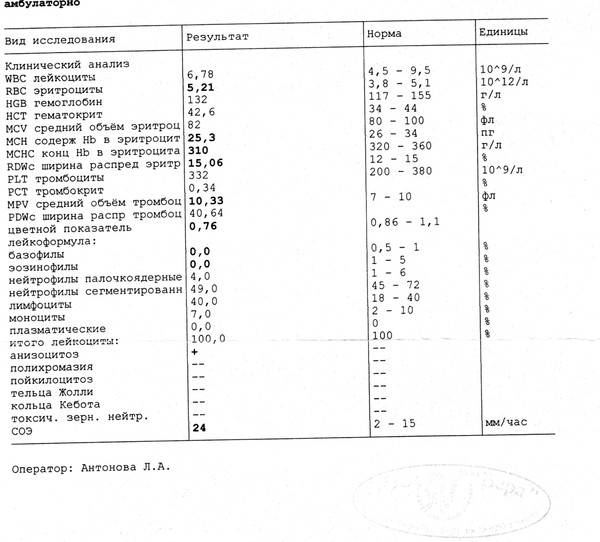
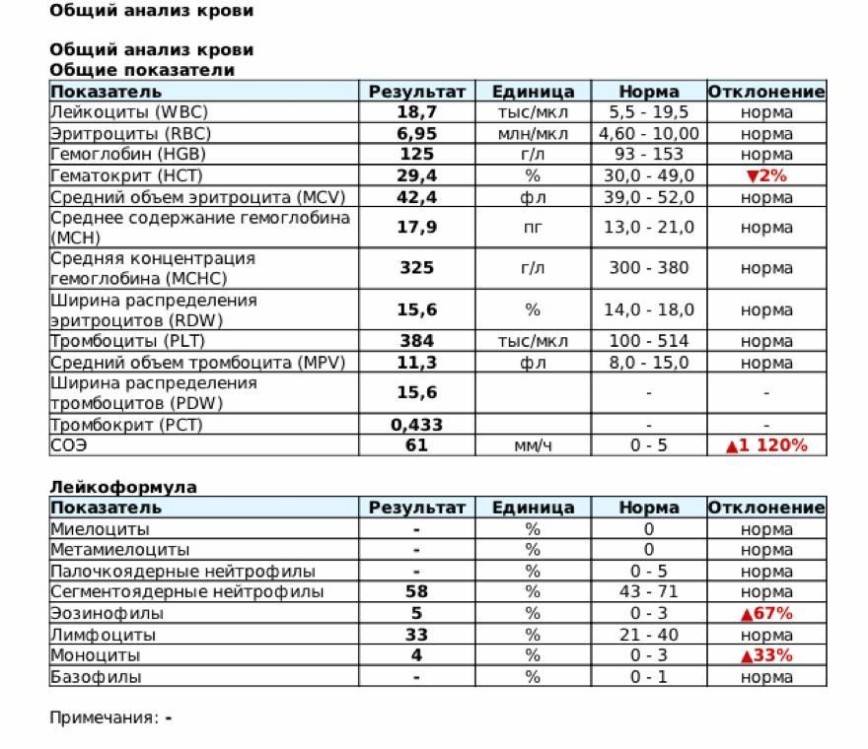
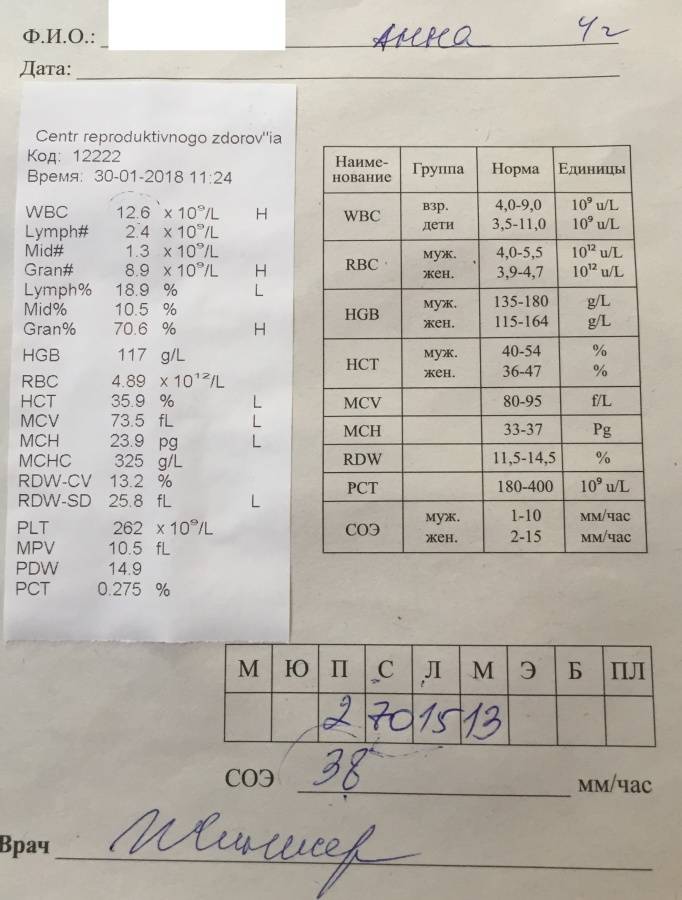
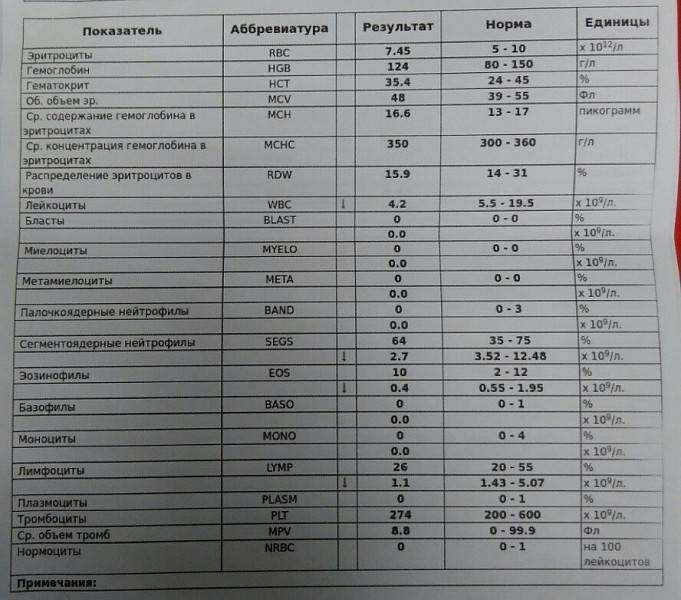
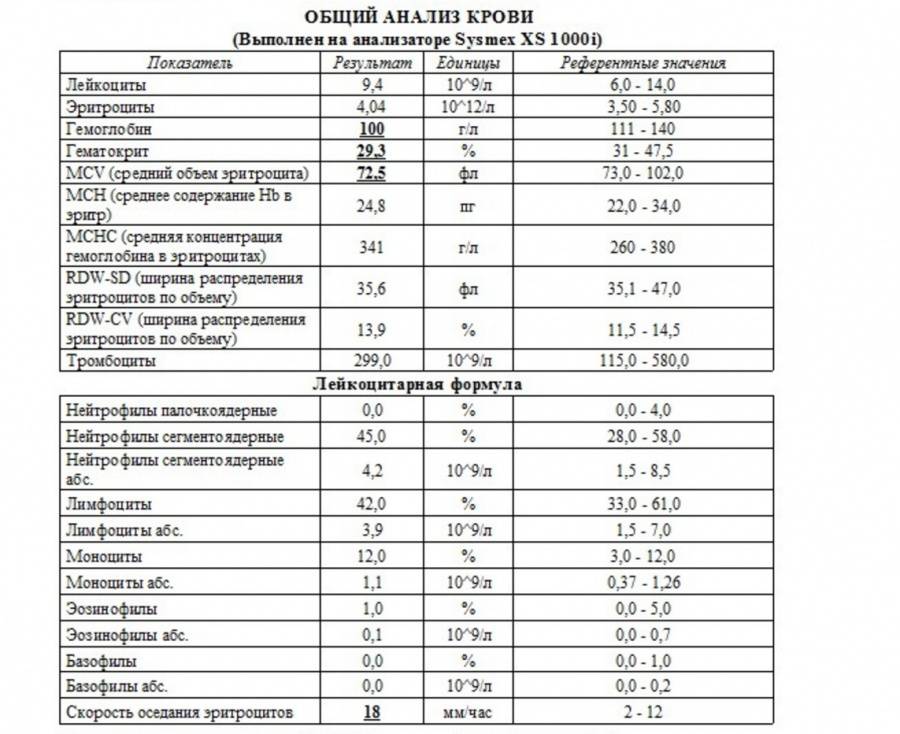
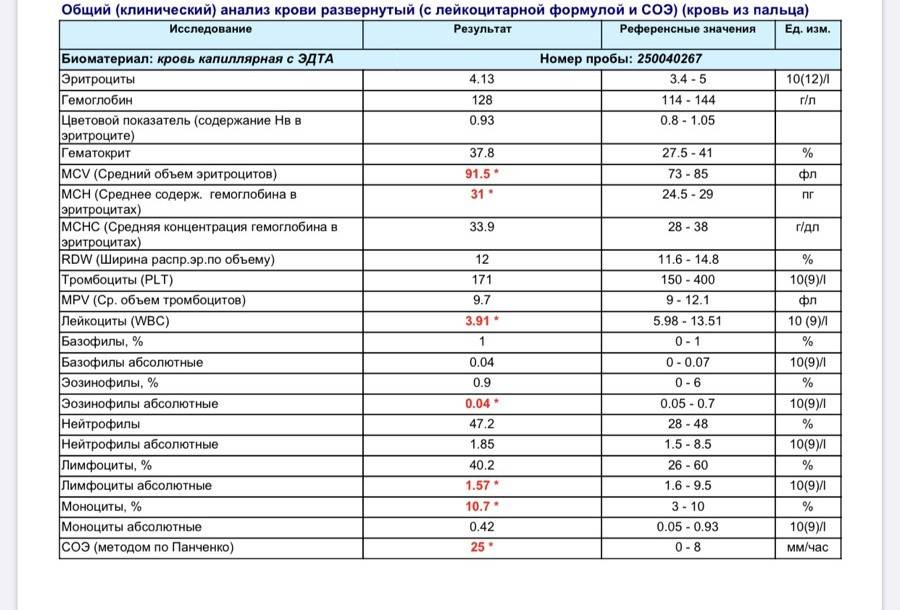
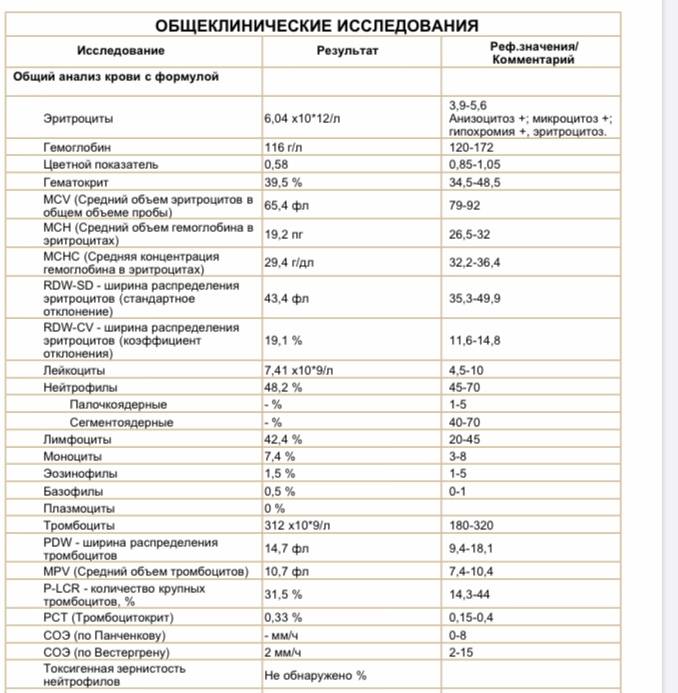
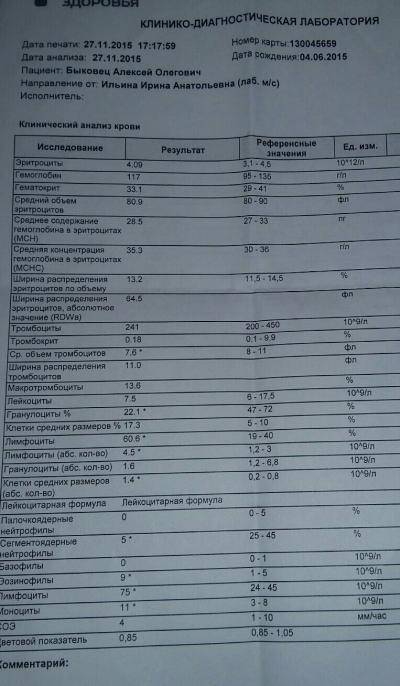
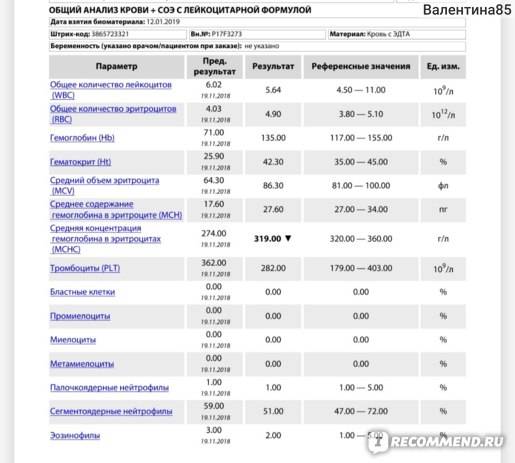
Общее количество лейкоцитов
| Лейкоциты – это живые клетки крови, которые формируют клеточный иммунитет всего организма. Эти клетки призваны бороться с инфекционными агентами, обезвреживать токсины и синтезировать антитела против чужеродных веществ и организмов. В группу лейкоцитов входят следующие виды: нейтрофилы, базофилы, эозинофилы, моноциты, лимфоциты. Все эти виды лейкоцитов выполняют различные функции и имеют различное строение. | |||||||||||||||||
| Почему повышены лейкоциты?Причины непатологического повышение уровня лейкоцитов
На фоне воспалительной реакции
| ||||||||||||||||
Почему понижены лейкоциты?
|
Определение и цели назначения
ОАК (общий анализ крови) – это способ лабораторной диагностики для оценки состояния организма и поиска источника патологии. Этот анализ может назначить врач любой специальности. В каких случаях назначается ОАК:
- Для профилактики на медицинских осмотрах. Состав крови относительно постоянен и крайне редко выходит за рамки границ нормы у здорового человека. А некоторые болезни могут долгое время не влиять на самочувствие, и тогда профилактическая сдача станет поводом для последующего обследования.
- При появлении первых симптомов недомогания. Анализ в этом случае может позволить определить природу болезни, степень интенсивности воспаления или аллергической реакции.
- ОАК могут назначить повторно, чтобы отследить течение болезни через определенное время. Также для оценки эффективности проводимой терапии.
Как берется кровь и нужна ли подготовка к процедуре?
Сдача крови – простая и практически безболезненная процедура, которую легко переносят даже грудные дети. Биологический материал для общего исследования берется преимущественно из пальца, но для проверки по расширенному списку параметров и в некоторых других случаях врачи назначают венозную пункцию.
Для предотвращения занесения инфекции и взятия чистого материала медсестра протирают подушечку одного из пальцев левой кисти смоченным в спирте тампоном. Сразу после этого специальным инструментом, скарификатором, наносят крошечный разрез около 3 мм глубиной. Выступающая из разреза кровь собирается пипеткой для забора и переливается в высокую пробирку. Небольшая часть жидкости мазком наносится на предметное стекло.
Если врачом назначена венозная пункция, на предплечье пациента накладывают резиновый жгут, замедляющий кровоток ниже перевязки. Затем место прокола на внутренней поверхности сгиба локтя дезинфицируют спиртом, после чего вводят в вену полую иглу. Сквозь неё кровь из сосуда наполняет специальную пробирку, а небольшое количество биоматериала наносится на предметное стекло.
Для проведения процедуры специальные приготовления не нужны. Единственное, о чем могут попросить врачи, — не завтракать перед забором биоматериала, так как употребление пищи может исказить полученные результаты.
В ряде случаев делать анализ приходится по нескольку раз за установленный временной отрезок, в том числе, для отслеживания результативности назначенного лечения. Чтобы получить наиболее точные данные для сравнения, повторная сдача крови проводится примерно в том промежутке времени, что и в первый раз.
Когда сдавать анализы при беременности
График сдачи анализов при беременности построен с учетом внутриутробного развития плода, поэтому важно сдавать их вовремя. Результаты некоторых, если сдать их позже, становятся неинформативными из-за сложности интерпретации результатов
Первые анализы женщина сдает при постановке на учет у акушера-гинеколога, а последующие согласно плану. Скрининговые анализы назначают в периоды с 12 по 14 неделю беременности, с 20 по 24 и с 30 по 32. В это же время делают и пренатальное УЗИ.
В обязательном порядке беременным назначают:
- Общий анализ крови;
- Анализ крови на сахар;
- Анализ крови на ХГЧ (хорионический гонадотропин человека);
- Анализ крови на группу и резус-фактор;
- Анализ крови на гормоны (ТТГ, Т4, прогестерон и другие);
- Анализ крови на торч-инфекции (вирус герпеса, гепатита, краснухи, волчанки, токсоплазмоза, цитомегаловируса);
- Анализ крови на ВИЧ;
- Анализ крови на сифилис (реакция RW);
- Анализ крови на определение ПАПП-белка;
- Двухчасовой тест толерантности к глюкозе;
- Общий анализ мочи;
- Бактериологическое исследование мочи на скрытые инфекции;
- Мазок на патогенную флору и цитологию.
Перечень назначенных врачом анализов может быть и другим. Например, некоторые он может отменить, если женщина уже сдавала их при планировании беременности. Также доктор может назначить и дополнительные исследования крови или инструментальные обследования. Часто проводят колькоскопию при беременности, которая позволяет оценить состояние шейки матки.
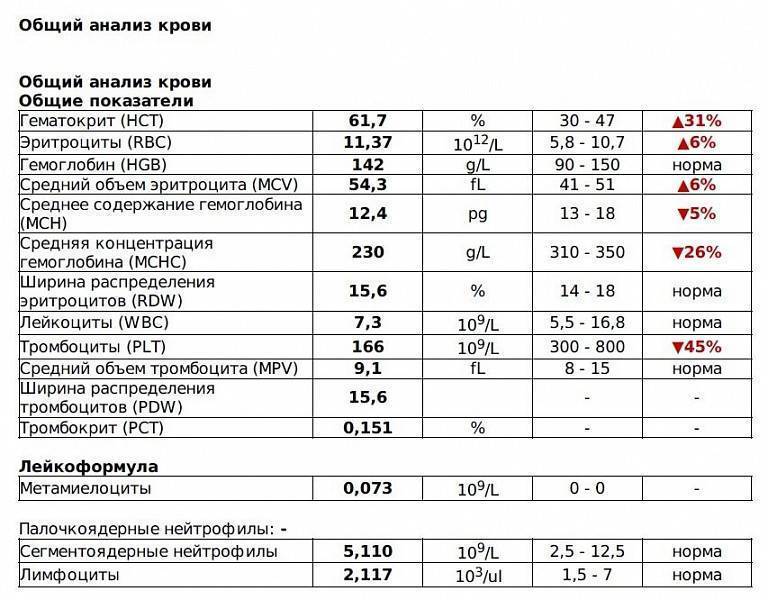
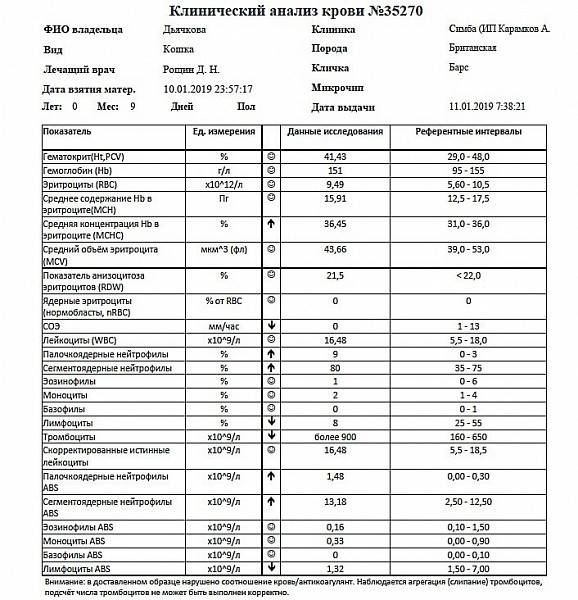
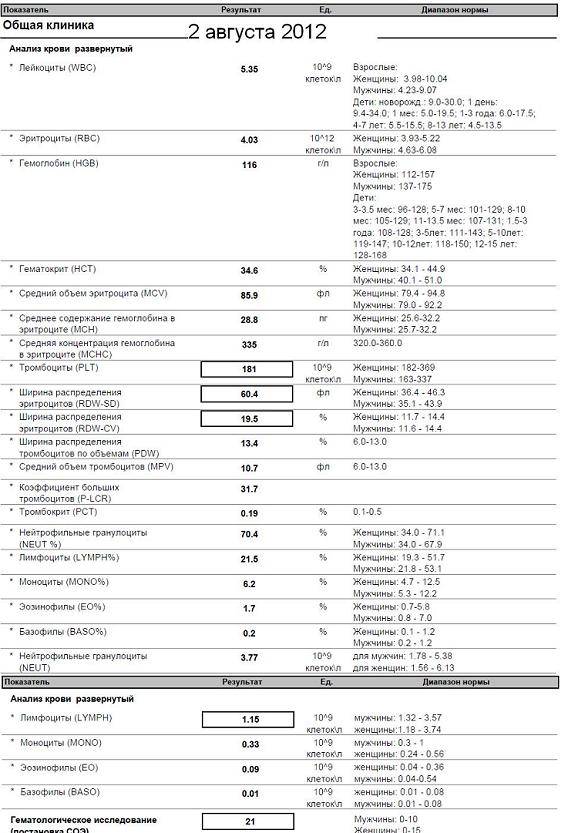
Тромбоциты
Основная задача тромбоцитов — участие в остановке кровотечений. Они образуют первичную пробку в области повреждения сосуда и участвуют в формировании кровяного сгустка. В бланках автоматических анализаторов обозначаются аббревиатурой PLT, которая происходит от английского слова platelets (буквально, “блюдца”) за их своеобразную форму.
Снижение числа тромбоцитов может сопровождаться кровотечениями и является следствием таких заболеваний и состояний, как малярия, тромбоцитопеническая пурпура, злокачественные новообразования, ДВС-синдром и некоторых других.
Высокий уровень тромбоцитов может стать причиной чрезмерного тромбообразования и нередко не имеет видимых причин. В таком случае состояние обозначается, как эссенциальная тромбоцитемия. Помимо этого причиной тромбоцитоза могут выступать железодефицитная анемия, гемолиз, некоторые инфекционные и аутоиммунные заболевания, поражение костного мозга.
Работа с тромбоцитами в классическом анализе крови на этом исчерпывается, однако, автоматические анализаторы и в этом случае предлагают дополнительные диагностические возможности в виде следующих показателей:
- MPV — средний объём тромбоцитов. Показатель, отражающий размеры клеток, которые напрямую зависят от их возраста. Повышенный MPV может свидетельствовать о гематологических заболеваниях, поражении селезенки, тиреотоксикозе, прогрессировании атеросклероза. Снижение показателя отмечается при некоторых генетических заболеваниях, инфаркта миокарда, детских инфекциях, химиотерапии рака и целого ряда других состояний.
- PCT — отношение общего объема тромбоцитов к плазме крови (тромбокрит). Не является специфическим показателем, широко колеблется физиологически, но позволяет оценить риск развития кровотечений и тромбозов.
- PDW — распределение тромбоцитов по объёму. Показатель не имеет самостоятельного значения и оценивается в связке с другими индексами.
Агранулоцитоз у детей
В развитии АГРАНУЛОЦИТОЗА у детей играют роль те же механизмы, что и у взрослых. Клиническая картина миелотоксического и иммунного АГРАНУЛОЦИТОЗА соответствует таковой у взрослых.
У детей в раннем возрасте сравнительно редко возникают своеобразные нейтропении, которые по клиническим особенностям, осложнениям во многом напоминают картину АГРАНУЛОЦИТОЗА. Известны два основных типа нейтропений: постоянная и периодическая.
Постоянная нейтропения, описанная Костманном, характеризуется возникновением в раннем детском возрасте повторяющихся гнойных заболеваний: абсцессов на коже, в легких, отитов и т. п. С появлением зубов развивается амфодонтоз, ведущий к раннему выпадению зубов. В крови отмечается нейтропения при нормальном или несколько сниженном количестве лейкоцитов. Показатели красной крови и тромбоцитов не изменены. Эта форма заболевания наследуется по рецессивному типу. Описаны единичные случаи аналогичного заболевания, протекающего более мягко, наследуемого доминантно . В костном мозге отмечается остановка созревания нейтрофилов на стадии промиелоцитов, повышенный процент моноцитов и эозинофилов.
Периодическая нейтропения характеризуется регулярными подъемами температуры, вспышками гнойных процессов, исчезновением зрелых нейтрофилов из крови и костного мозга. Нейтропенический период продолжается несколько дней, затем восстанавливается нормальная картина крови. В период нейтропении картина крови и костного мозга соответствует таковой при постоянной форме. В большинстве случаев болезнь наследуется по рецессивному типу [Пейдж (Page) с сотр., Видебек, реже по доминантному.
Наряду с наследственными формами описана и преходящая врожденная нейтропения [Стефанини (М. Stefanini)) у грудных детей, матери которых страдают гранулоцитопенией.
Лечение агранулоцитоза у детей проводится по тем же правилам, что и у взрослых. В лечении наследственных нейтропений важнейшая роль принадлежит антибиотикам, которые назначают при периодической форме за 2—3 дня до ожидаемого криза на весь период нейтропении. При постоянной нейтропении антибиотическая терапия проводится в связи с гнойными осложнениями. Ведущее место принадлежит противостафилококковым препаратам, а также антибиотикам широкого спектра действия: оксациллину, метициллину, цепорину и другие. С введением массивной антибиотической терапии резко снизилась летальность в первые годы жизни — наиболее опасный период болезни; в дальнейшем заболевание протекает несколько мягче, больные доживают до зрелого возраста. Кроме общей терапии, проводится систематическая санация полости рта, уход за деснами.
Библиография: Александер Г. Л. Осложнения при лекарственной терапии, пер. с англ.. М., 1958, библиогр.; Аллергии и аллергические заболевания, под ред. Э. Райка, пер. с венгер., т. 1—2, Будапешт, 1966; Движков П. П. Агранулоцитоз, Клии. мед., т. 6, Xj 14, с. 1000, 1928, библиогр.; Доссе Ж. Иммуногематология, пер. с франц., с. 590, М., 1959; И с т а-манова Т. С. и Алмазов В. А. Лейкопении и агранулоцитозы, Л., 1961, библиогр.; Л а в к о в и ч В. и Кржеминьска-Лавкович И. Гематология детского возраста, пер. с иольск., с. 218, Варшава, 1964; Мешлин С. Агранулоцитоз, обусловленный повышенной чувствительностью к лекарственным препаратам, в кн.: Аллергия к лекарствен, веществам, под ред. М. Л. Розенхейма и Р. Моултона, пер. с англ., с. 116, М., 1962, библиогр.; Тур А. Ф. Гематология детского возраста, Л., 1963, библиогр.; Воск Н. Е. Thcrapie dcr Agranulozytose, Dtsch. med. Wschr., S. 1722, 1965; Handling of radiation accidents, Vienna, 1969, bibliogr.; Ingоld J. A. Radiation hepatitis, Amcr. J. Roentgenol., v. 93, p. 200, 1965, bibliogr.; Mathd G. Prevention ct trai-tement des aplasies глёдыНа^гев, Concours m6d., p. 3319, 1969; Perlmutter R. A. Hepatitis and aplastic anemia, Calif. Med., v. 110, p. 135, 1969, bibliogr.; Whitby L. E. H. a. Вrittо и 0. J. C. Disorders of the blood, L., 1957, bibliogr.; Wick A. Zur Prognose und Therapic der Agranulozytose, Schweiz, med. Wschr., S. 357, 1963, Bibliogr.
НЕТРЕПОНЕМНЫЕ ТЕСТЫ
Реакция Вассермана- РВ, RW, в среднем, становится положительной на 4-6 неделе заболевания. С увеличением поступления возбудителя сифилиса в кровь растет и титр RW. Своего максимума он достигает во вторичном рецидивном периоде сифилиса. При поздних формах заболевания реакция Вассермана нередко становится отрицательной.
Результат реакции Вассермана определяется наличием или отсутствием гемолиза. RW резко положительная – ++++, полная задержка гемолиза, RW положительная -+++, значительная задержка гемолиза, слабоположительная rw -++, +- сомнительная RW- частичная и соответственно незначительная задержка гемолиза. Отрицательная RW – полный гемолиз.
Недостатком RW является ее неспецифичность, т.е. реакция Вассермана становится положительной при отсутствиии сифилиса. Такой анализ называется ложноположительный.
Реакция Вассермана может быть ложноположительной при различных заболеваниях и состояниях – болезни соединительной ткани ( системная красная волчанка, системная склеродермия, дерматомиозит), ревматоидный артрит, туберкулез, онкология, болезни крови, заболевания сердечно-сосудистой системы – инфаркт миокарда, сахарный диабет, заболевания почек, беременность , употребление лекарственных препаратов и т.д.
Из-за неспецифичности реакции Вассермана, ее ложных результатов также используются другие реакции.
Реакция микропреципитации (РМП) и ее аналоги: RPR тест – Rapid Plasma Reagins и тест VDRL (Venereal Diseases Research Laboratory) – это нетрепонемные тесты, которые широко применяются в качестве отборочных реакций на сифилис.
Реакцию микропреципитации целесообразно сдавать через 20-30 дней после опасного контакта.
Суть реакции РМП – несколько капель сыворотки крови обследуемого смешивается с кардиолипиновым антигеном, в ходе реакции выпадает осадок – преципитат. Реакция оценивается качественно – по количеству +, от 4+(резко положительный) результат, до1+(сомнительный результат). В случае положительного результата проводят количественную оценку – титрование – максимальное разведение, при котором образуется осадок-преципитат. Результат является положительным начиная с титра 1:2-1:4. В подавляющем большинстве случаев положительный результат микрореакции означает заболевание сифилисом. Однако, микрореакция бывает ложноположительной при системных заболеваниях – системная красная волчанка, ревматоидный артрит, гломерулонефрит, сахарный диабет; при онкологических процессах, заболеваниях сердца – острый инфаркт миокарда, эндокардит, миокардит; при беременности и т.д.
Отрицательный результат микрореакции свидетельствует об отсутствии сифилиса, о раннем серонегативном периоде заболевания, до появления антител в крови. Также микрореакция становится отрицательной или сомнительной при поздних формах сифилиса.
Акция!!! Анализ крови на сифилис, ВИЧ, СПИД, гепатиты – 2500 руб.!
Телефон: 8 985 9230340
РМП является одним из критериев достоверности проведенного лечения сифилиса. В отличие от других серологических реакций – РИФ, РИБТ, ИФА, РПГА, после успешного лечения сифилиса РМП становится отрицательной более чем в 90% случаев.
Нетрепонемные тесты (реакция микропреципитации (РМП) и реакция Вассермана (RW)) относятся к неотъемлемым методам диагностики сифилиса. Отрицательный результат этих реакций в подавляющем большинстве случаев означает, что обследуемый здоров. В противном случае, при получении положительных результатов анализов назначаются трепонемные тесты.
Клиническая картина
Миелотоксический АГРАНУЛОЦИТОЗ начинается исподволь: без каких-либо субъективных признаков. Иммунный АГРАНУЛОЦИТОЗ клинически может иметь различные варианты в зависимости от вызвавшего его фактора. АГРАНУЛОЦИТОЗ на фоне коллагеноза развивается постепенно и отличается упорством течения. Начало медикаментозного иммунного АГРАНУЛОЦИТОЗА в большинстве случаев острое.
Первыми проявлениями любого АГРАНУЛОЦИТОЗА являются лихорадка, стоматит, ангина. При миелотоксическом синдроме отмечается и обычно умеренно выраженный геморрагический синдром (синяки и кровоточивость десен, носовые кровотечения): выраженный геморрагический синдром — нечастое осложнение АГРАНУЛОЦИТОЗА Поражение слизистых оболочек (некрозы и молочница) полости рта и желудочно-кишечного тракта — наиболее постоянный признак АГРАНУЛОЦИТОЗА. При миелотоксическом АГРАНУЛОЦИТОЕ оно обусловлено тем, что, с одной стороны, исчезновение гранулоцитов делает возможной микробную инвазию, с другой — подавление митозов эпителиальных клеток слизистой оболочки цитостатическими факторами нарушает ее целостность.
В периферической крови уменьшается количество всех форм лейкоцитов (нередко до сотен клеток в 1 мкл), а также тромбоцитов и ретикулоцитов. Число плазматических клеток обычно увеличено. Может быть анемия. Иногда гранулоциты исчезают полностью. Лейкопения при иммунном АГРАНУЛОЦИТОЗЕ носит умеренный характер — 1000—2000 клеток в 1 мкл, но количество гранулоцитов, как правило, уменьшается до нуля; тромбоцитопения отсутствует. В сыворотке обнаруживаются антилейкоцитарные антитела.
На высоте миелотоксического АГРАНУЛОЦИТОЗА в костном мозге почти полностью исчезают как гранулоцитарные элементы, так и эритронормобласты, мегакариоциты; лимфоидные, ретикулярные и плазматические клетки сохраняются. За 2—3 дня до выхода из состояния АГРАНУЛОЦИТОЗА в костном мозге появляются в огромном количестве промиелоциты и единичные нормобласты. В периферической крови первым признаком активации кроветворения является обнаружение молодых элементов — миелоцитов и метамиелоцитов, иногда плазматических клеток. Часто за 2—3 дня до появления гранулоцитов увеличивается число тромбоцитов и ретикулоцитов.
В костном мозге при иммунном АГРАНУЛОЦИТОЗЕ отмечается уменьшение клеточных элементов исключительно за счет гранулоцитарного ростка. Выход из иммунного АГРАНУЛОЦИТОЗА характеризуется появлением в периферической крови молодых клеток — миелоцитов, метамиелоцитов, иногда промиелоцитов.
Продолжительность АГРАНУЛОЦИТОЗА различна и зависит как от степени поражения костного мозга, так и от индивидуальных особенностей организма больного.
Бактерии в моче:
Дрожжевые грибки Обнаружение дрожжей рода Кандида свидетельствует о кандидамикозе, возникающего чаще всего в результате нерациональной антибиотикотерапии.
Референсные значения: отрицательно
2.6. Неорганический осадок мочи (кристаллы), соли в мочеМоча – это раствор различных солей, которые могут при стоянии мочи выпадать в осадок (образовывать кристаллы). Образованию кристаллов способствует низкая температура. Наличие тех или иных кристаллов солей в мочевом осадке указывает на изменение реакции в кислую или щелочную сторону. Избыточное содержание солей в моче способствует образованию конкрементов и развитию мочекаменной болезни. В тоже время диагностическое значение присутствия в моче кристаллов солей обычно невелико. К образованию кристаллов ведут повышенные дозы ампициллина, сульфаниламидов.
Мочевая кислота в физиологических условиях встречается при большой концентрации мочи, после обильной мясной пищи, после обильного потоотделения.
Референсные значения: отсутствуют
Мочевая кислота и ее соли (ураты):
- высококонцентрированная моча;
- кислая реакция мочи (после физической нагрузки, мясной диете, лихорадке, лейкозах);
- мочекислый диатез, подагра;
- хроническая почечная недостаточность;
- острый и хронический нефрит;
- обезвоживание (рвота, понос);
- у новорожденных.
Кристаллы гиппуровой кислоты:
- употребление в пищу плодов, содержащих бензойную кислоту (черника, брусника);
- диабет;
- болезни печени;
- гнилостные процессы в кишечнике.
Аммиак-магнезии фосфаты, аморфные фосфаты:
- щелочная реакция мочи у здоровых;
- рвота, промывание желудка;
- цистит;
- синдром Фанкони, гиперпаратиреоз.
Оксалат кальция (оксалурия встречается при любой реакции мочи):
- употребление в пищу продуктов, богатых щавелевой кислотой (шпинат, щавель, томаты, спаржа, ревень);
- пиелонефрит;
- сахарный диабет;
- отравление этиленгликолем.
Лейцин и тирозин:
- выраженное расстройство обмена веществ;
- отравление фосфором;
- деструктивные заболевания печени;
- пернициозная анемия;
- лейкоз.
Цистин:
врожденное нарушение цистинового обмена – цистиноз.
Жир и жирные кислоты:
- дегенеративные изменения эпителия почечных канальцев;
- употребление в пищу большого количества рыбьего жира.
Холестерин:
- хилурия;
- жировое перерождение почек;
- эхинококкоз почек;
- цистит;
- холестериновые камни.
Билирубин:
- гепатиты;
- рак печени;
- инфекционные заболевания;
- отравление фосфором.
Гематоидин:
хронические кровотечения на протяжении мочевыводящего тракта, особенно если кровь где-либо застаивается.
2.7. Слизь в мочеСлизь выделяется эпителием слизистых оболочек. В норме присутствует в моче в незначительном количестве. При воспалительных процессах содержание слизи в моче повышается. Увеличенное количество слизи в моче может говорить о нарушении правил правильной подготовки к взятию пробы мочи.
Референсные значения: незначительное количество.
UBG – уробилиногенBIL биллирубин KET кетоновые тела CRE креатинин BLD эритроциты PRO белок MALB – микроальбумин должен быть меньше 20 мг на литр NIT Нитриты LEU лейкоцитыGLU глюкозаSG удельный вес pH кислотность VC витамин С A:C соотношение альбумина и креатининаNeg – отсутствие показателя
Московский детский центр лабораторной диагностики осуществляет приём на исследования ЕЖЕДНЕВНО, кроме субботы и воскресенья, с 8.30 час. до 11.30 час., 2 корпус, 3 этаж.Тел.: 8 (499) 254-0910; 8 (499) 254-2110; 8 (499) 254-6740.Результаты анализов Вы можете получить, оставив свою электронную почту.
Платные лабораторные исследования можно провести как ребёнку, так и родителям.
Процедурный кабинет находится в 15 корпусе, 3 этаж, кабинет № 307, работает с 9.00 час. до 13.00 час.
Оплата производится:– в 15 корпусе, 5этаж, кабинет № 511;- в 11 корпусе, 1 этаж, кабинет № 106.
Прогнозировование и факторы риска при миеломе
«Международная система прогнозирования» (ISS. 2005) была разработана на основании данных естественного исхода заболевания значительной клинической группы больных и основана на исследовании бета-2 микроглобулина в динамике. Бета-2 микроглобулин повышен у 75% больных миеломной болезнью.
Выделено три уровня этого онкомаркера, которые связаны с длительной выживаемостью пациентов. Это позволяет определить несколько стадий заболевния.
- бета-2-микроглобулин менее 3,5 мг/л и альбумин более 35 г/л, средняя выживаемость 62 месяца,
- промежуточная между 1 и 3 стадиями, средняя выживаемость 44 месяца.
- бета 2-микроглобулин более 5.5 мг/л, средняя выживаемость 29 мес.
Однако, в настоящее время использование новых препаратов значительно изменило прогноз естественного течения заболевания. Тем не менее, международная система была протестирована для новейшей терапии и подтвердила свою надежность. Так, 5-летняя выживаемость больных в стадии I, II и III составила 66%, 45% и 18% соответственно.
В Международной системе не оказалось места для таких ценных прогностических показателей как число тромбоцитов, уровень лактатдегидрогеназы и свободных легких цепей в крови.
Число тромбоцитов в крови коррелирует с вытеснением костного мозга и имеет предсказательное значение выше, чем у альбумина. Содержание лактатдегидрогеназы (ЛДГ) коррелирует с общей массой миеломных клеток, недостаточным ответом на терапию и укорочением выживаемости. У больных с уровнем свободных легких цепей в крови свыше 4,75 г/л чаще выявляется почечная недостаточность, высокой процент миеломных клеток в пунктате костного мозга, высокие значения бета-2-микроглобулина и лактатдегдрогеназы, чаще обнаруживается болезнь отложения легких цепей и стадия III по Международной системе. Однако представленных доказательств оказалось недостаточно, чтобы включить эти три критерия в Международную систему. Но они были представлены в системе Дьюри-Саймона (1975), значение которой не оспаривается до сих пор.
Повышенный уровень сывороточного бета 2-микроглобулина, повышенный уровень лактатдегидрогеназы и низкий уровень сывороточного альбумина относятся к неблагоприятным признакам прогноза при миеломной болезни. Хотя уровень бета-2- микроглобулина увеличивается при почечной недостаточности, существует значительная корреляция между объемом опухолевой ткани и концентрацией этого биомаркера в крови. Исключение составляют лишь случаи, когда миеломная болезнь развивается уже на фоне имеющейся почечной недостаточности.
Перспективным методом оценки прогноза заболевания является генетическое исследование опухоль-ассоциированных генов. Цитогенетическое выявление транслокаций в отличие от трисомии относится к неблагоприятным прогностическим признакам. Метод флюоресцентной гибридизации in situ (FISH) позволил упростить выявление хромосомных аберраций в миеломных клетках, что предлагается исследователями клинико Мэйо (США) использовать для выбора индивидуальной лечебной тактики, исходя из прогноза для больного на основании учета выявленных аберраций. Генетические исследования хромосомных аномалий и мутаций при миеломе являются перспективными методами для лабораторной оценке прогноза и устойчивости к терапии при миеломе. Однако для их оценки требуются большие сроки и число пролеченных больных, чтобы определить способность новых средств терапии преодолеть цитогенетические показатели высокого риска при миеломной болезни.
Химические свойства
Белок. В норме его в моче быть не должно, или там очень мало — меньше 0,002 г/л. Иногда у здоровых людей он все-таки появляется — например, если они поели мяса, или испытали накануне серьезную физическую нагрузку или эмоциональный стресс — но если человек перестает есть мясо, отдыхает и успокаивается, выделение белка прекращается. Если он продолжает выделяться вместе с мочой (это устанавливают, повторяя анализ снова и снова), дело может быть в воспалении почек или мочевыводящих путей.
Глюкоза. У здоровых небеременных людей глюкозы в моче быть не должно. Как мы уже писали, «сахар» попадает в мочу при нарушениях обмена глюкозы — например, при диабете II типа.
Кетоновые тела. Эти вещества накапливаются в организме, если телу не хватает углеводов, и для получения энергии оно вынуждено разрушать запасы жира. Поскольку питаться ими для нас не нормально, кетоновых тел в моче здоровых небеременных людей быть не должно. Как правило, кетоновые тела появляются в моче у голодающих людей или из-за тяжелых физических нагрузок, но чаще всего — на фоне неконтролируемого диабета 1 типа.
Билирубин. У здоровых небеременных людей билирубина в моче быть не должно. Как мы уже писали, билирубин попадает в мочу, если печень не справляется с его утилизацией. Такое бывает при гепатитах и при нарушении оттока желчи — это может случиться, если желчевыводящие пути, например, перекроет желчный камень.
Уробилиноген. Это бесцветный продукт «обезвреживания» вредного билирубина печенью и кишечными бактериями. До 10 мг/л уробилиногена выводится вместе с мочой. Если уровень этого вещества высокий, велика вероятность, что у человека проблемы с печенью — от вирусного гепатита до печеночной недостаточности. Но не исключено, что дело в ускоренном распаде гемоглобина — такое бывает, например, при гемолитической анемии и некоторых других заболеваниях.
Нитриты. Вместе с мочой организм избавляется от соединений азота — нитратов, так что они всегда в ней есть у здоровых людей. Но если в мочевыводящих путях поселяются болезнетворные бактерии — например, кишечные палочки, энтеробактерии или клебсиеллы — в моче появляются нитриты. Дело в том, что эти бактерии питаются нитратами и превращают их в нитриты, так что присутствие этих веществ в моче всегда недобрый знак. При этом отсутствие нитритов не означает отсутствие инфекции. Некоторые стафилококки и стрептококки к нитратам равнодушны, так что их приходится выявлять, просматривая мочу под микроскопом.