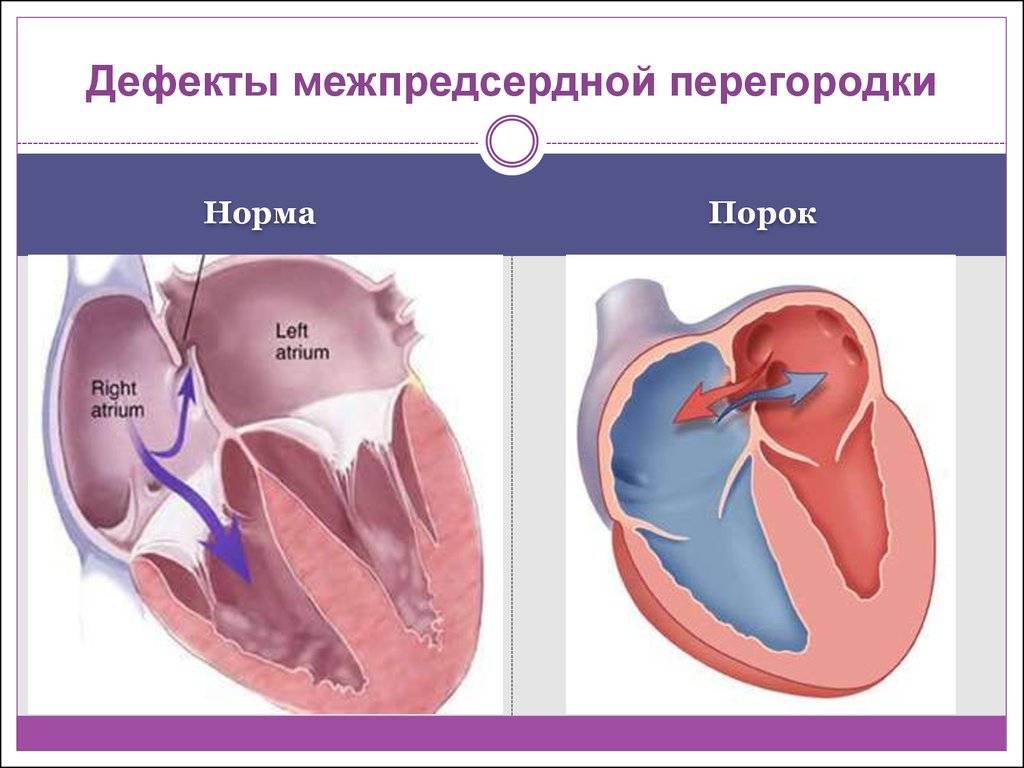
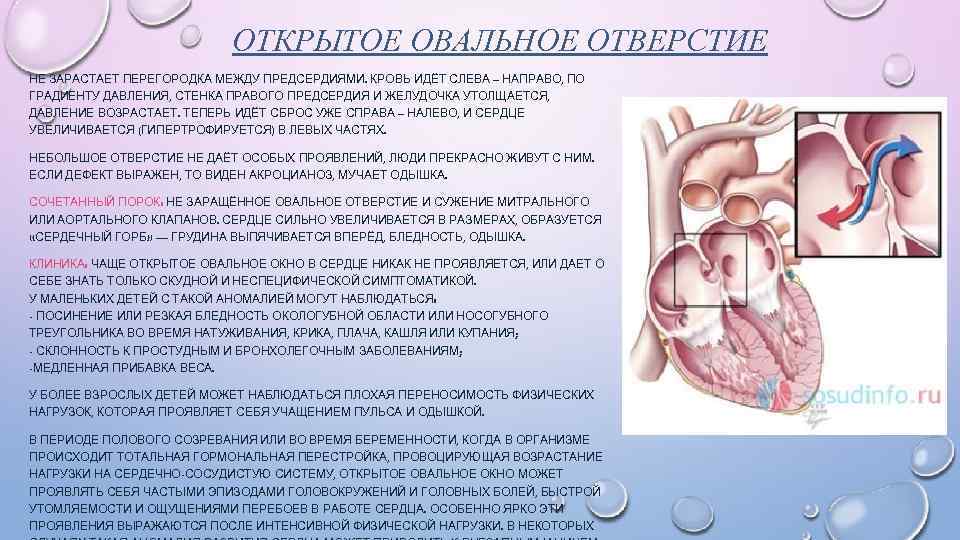
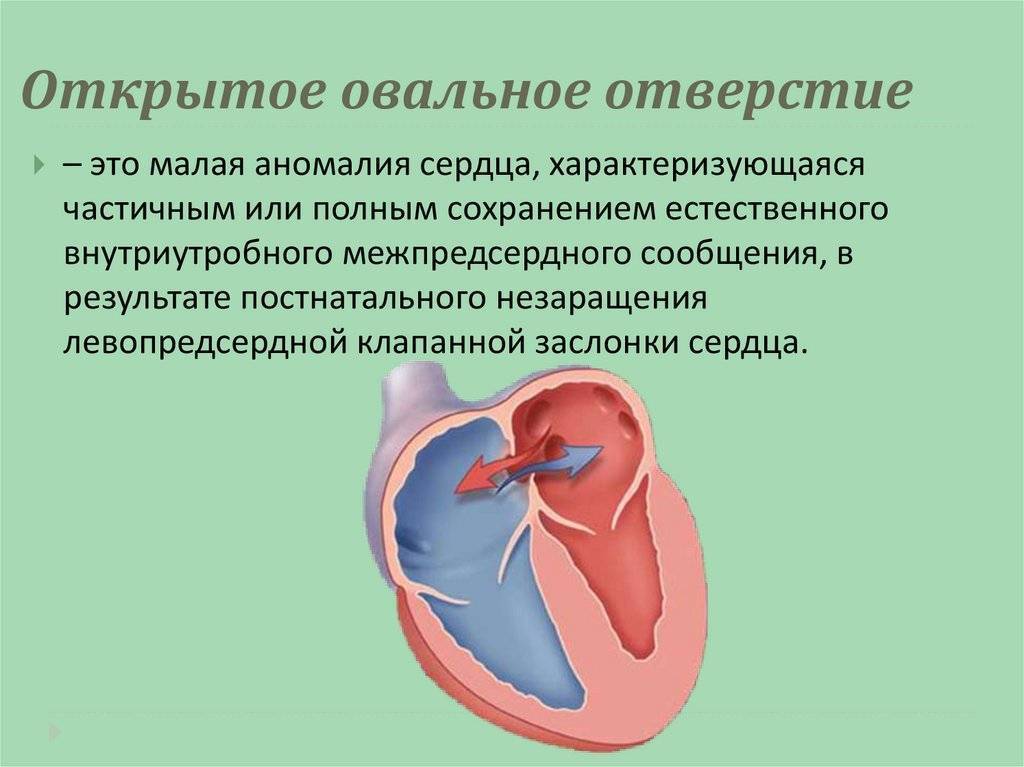
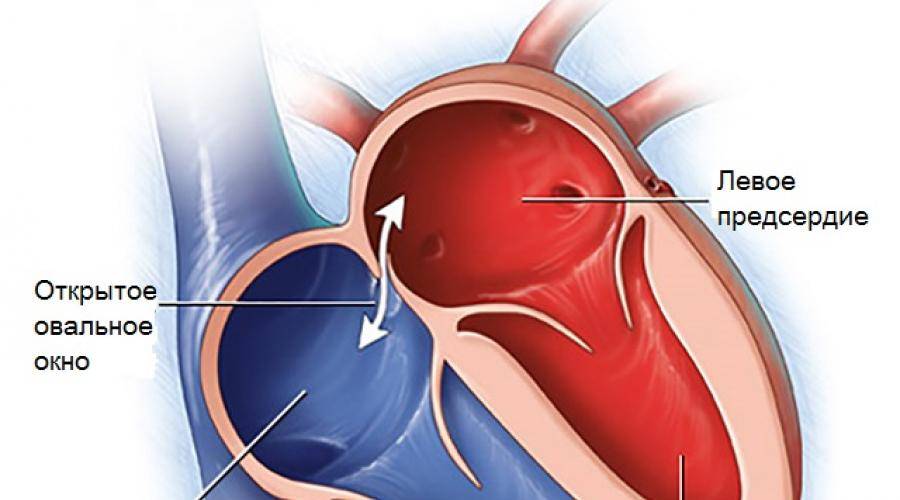
Терапия
Основным выбором в терапии заболевания является хирургическое закрытие ОАП.Методики закрытия ОАП развиваются начиная с первого сообщения наложения лигатуры Gross и Hubbard в 1939 году. Приоритет в закрытии ОАП отдается малоинвазивным, транскатетерным методикам, начало которым положили работы Portsmann и Ivalon в 1967 году. Результаты транскатетерной обструкции ОАП превосходные. Общая частота закрытия при длительном наблюдении превышает 90-95% в большинстве исследований . Даже когда сохраняется маленькое остаточное шунтирование, полная обструкция может быть достигнута в дальнейшем размещением дополнительного устройства . Серьезные осложнения транскатетерного закрытия ОАП являются редкими. Самое частое осложнение – эмболизация окклюдером, что относительно часто наблюдалось в ранних исследованиях. Другие потенциально важные осложнения – турбуленция потока в проксимальной части левой легочной артерии или нисходящей аорте от выпирающего устройства, гемолиз при высокоскоростном резидуальном шунтировании, тромбоз бедренной артерии или вены, связанный с сосудистой инфекцией. Хирургические операции с наложением лигатуры или разделением ОАП остаются терапией выбора для очень больших протоков. Редко большой проток по типу аортолегочного окна может иметь недостаточную длину, чтобы разместить лигатуру, поэтому соответствующим хирургическим вмешательством является наложение заплаты . Общая частота эффективности хирургического закрытия в опубликованных отчетах располагаются от 94 до 100%, с 0-2%-ной смертностью . Серьезные осложнения включают кровотечение, пневмоторакс, инфекцию и, редко, наложение лигатуры на левую легочную артерию или аорту .
Считается, что закрытие ОАП показано у любого ребенка или взрослого, у которого развивается симптоматика в результате шунтирования. У бессимптомных пациентов с существенным шунтированием слева направо, сопровождающегося увеличением левых отделов, закрытие протока показано, чтобы снизить риск последующих осложнений . У пациентов с синдромом Эйзенменгера после закрытия протока может наблюдаться ухудшение гемодинамики в результате утраты сброса крови справа налево и еще большего повышения давления в легочной артерии, что сопровождается снижением сердечного выброса и нарастанием правожелудочковой недостаточности.
Профилактика инфекционного эндокардита рекомендуется у всех лиц с функционирующим протоком, а также у лиц с остаточным, послеоперационным шунтированием .
В отношении тактики ведения немых протоков существует определенный разброс во мнениях. Некоторые авторы предлагают считать немой ОАП вариантом нормального физиологического развития, так же, как, тривиальную митральную регургитацию, которая не требует никакой терапии . С другой стороны, описаны случаи инфекционного эндартериита немого протока , поэтому таким пациентам может быть предложена не только профилактика инфекционного эндокардита, но и транскатетерное закрытие, особенно у молодых людей .
Таким образом, при общем благоприятном прогнозе тактика дальнейшего ведения больных с немым ОАП остается не совсем ясной, что требует дальнейшего обобщения данных результатов наблюдения, а возможно, и проведения крупномасштабного исследования .
Литература
1. И.Н. Митина, Ю.И. Бондарев. Неинвазивная ультразвуковая диагностика врожденных пороков сердца. Атлас. М. Видар-М. 2004.
2. Х. Фейгенбаум. Эхокардиография. 5-е издание. М. Видар. 1999.
3. Н. Шиллер, М.А. Осипов. Клиническая эхокардиография. Второе издание. М. Практика. 2005.
4. Caplin J.L. Small ductus arteriosus. Heart 1993; 70;98.
5. Deanfield J., Thaulow E., Warnes C., et al. The Task Force on the Management of Grown Up Congenital Heart Disease of the European Society of Cardiology. Eur Heart J 2003; V24 (N11): 1035-1084.
6. Houston A.B., Gnanapragasam J.P., Lim M.K., et al. Doppler ultrasound and the silent ductus arteriosus. Heart 1991; 65; 97-99.
7. Houston A., Hillis S., Lilley S., et al. Echocardiography in adult congenital heart disease. Heart 1998; 80 (Suppl 1): S12-S26.
8. Parthenakis F.I., Kanakaraki M.K., Vardas P.E. Silent patent ductus arteriosus endarteritis. Heart 2000; 84:619.
9. Schneider D.J., Moore J.W. Patent Ductus Arteriosus. Circulation 2006; 114:1873-1882.
Положение об отделении реанимации и интенсивной терапии новорожденных
I. Общее положение.1.1 Отделение реанимации и интенсивной терапии новорожденных (ОРИТН) организовано в составе Областного клинического перинатального центра (ВОКПЦ № 1) и является его структурным подразделением.1.2 В ОРИТН осуществляется оказание экстренной и плановой лечебной помощи новорожденным, рожденным в ВОКПЦ № 1 и переведенным из других лечебных учреждений области.1.3 Деятельность отделения реанимации и интенсивной терапии новорожденных регламентируются соответствующими нормативными документами, локальными нормативными актами, приказами по учреждению.
II. Цель и задачи отделения реанимации и интенсивной терапии новорожденных.2.1 Основной задачей ОРИТН является снижение перинатальной заболеваемости и смертности за счет:- оказания высококвалифицированной помощи новорожденным, требующим поддержания жизненно важных функций и проведения интенсивной терапии, включая пациентов с хирургической патологией в предоперационном периоде;- обеспечения санитарно-противоэпидемических. мероприятий на современном уровне и профилактика госпитальной инфекции;- проведения санитарно-просветительской работы с матерями и родственниками новорождённых и оказание эмоциональной поддержки родителям больных детей.2.2 Оказание практической, учебно-методической помощи врачам неонатологам и анестезиологам-реаниматологам районов области.2.3. Анализ дефектов при оказании помощи новорожденным в ВОКПЦ № 1 и районах Волгоградской области.2.4. Постоянная взаимосвязь с организационно-методическим отделом, дистанционно- консультативным центром с выездной анестезиологореанимационной неонатальной бригадой скорой медицинской помощи и РКЦ Областной детской больницы.
III. Структура отделения реанимаиии и интенсивной терапии новорожденных.3.1. Руководство отделением осуществляет заведующий, назначаемый и освобождаемый от занимаемой должности руководителем учреждения в установленном порядке.3.2. Заведующий отделением непосредственно подчиняется заместителям главного врача по анестезиолого-реанимационной и педиатрической помощи.3.3. Штаты отделения устанавливаются в соответствии с действующими нормативными документами с учетом местных условий или рассчитываются в соответствии с профилем и уровнем учреждения.3.4. Медицинский персонал в своей работе руководствуется должностными инструкциями, утвержденными главным врачом учреждения.
IV. Функции отделения реанимации и интенсивной терапии новорожденных.1. Оказание лечебно-диагностической помощи новорожденным:- мониторинг новорожденного на протяжении критических периодов ранней адаптации;- лабораторное и инструментальное исследование;- лечебно-охранительный режим и не агрессивные методы терапии;- оптимизация функций жизнеобеспечения;- индивидуализация и оптимизация интенсивной терапии;- этапность оказания интенсивной помощи новорожденным на ее различных уровнях;2. Организационно-методическая:- оказание практической, учебно-методической помощи врачам неонатологам и анестезиологам-реаниматологам районов области на рабочем месте, в отделении;- анализ историй болезни новорожденных с экспертной оценкой, родившихся в ОКПЦ и районах области;- анализ основных показателей работы отделения ежемесячно, ежеквартально;- оказание лечебно-консультативной помощи врачам неонатологам ВОКПЦ № 1;- участие в контрольно-экспертных комиссиях по перинатальной заболеваемости и смертности;3. Аналитическая функция:- оперативный и плановый анализ показателей перинатальной заболеваемости и смертности в ВОКПЦ № 1, совместно с информационно-аналитическим центром ОКПЦ и сотрудниками кафедры ФУВ ВолГМУ;- анализ дефектов лечения и обследования новорожденных в ОРИТН;
V. Критерии качества работы ОРИТН.- ранняя неонатальная смертность в ВОКПЦ № 1;- неонатальная смертность в ВОКПЦ № 1;- летальность по отделению, отдельно в группе доношенных и недоношенных;- заболеваемость госпитальной инфекцией в отделений;- летальность среди новорожденных находившихся на ИВЛ;- удельный вес пролеченных на продленной ИВЛ в различных весовых категориях (доношенные, недоношенные);- процент внутрижелудочных кровоизлияний, ретинопатия новорожденных и бронхолегочной дисплазии среди недоношенных детей;- выживаемость детей с очень низкой и экстремально низкой массой тела;- койко-день;- удельный вес расхождений диагнозов по данным патологоанатомических вскрытий.- учет перегоспитализированных новорожденных.
Тетрада Фалло
Тетрада Фалло – сложный порок сердца, состоящий из четырех аномалий– сужения легочной артерии, неправильного правостороннего положения аорты, расширения правого желудочка и дефекта межжелудочковой перегородки и вторично развивающейся гипертрофии правого желудочка. Все эти пороки могут быть выражены в разной степени. Это один из самых часто встречающихся синих (сопровождающихся цианозом) врожденных пороков сердца. Его частота 10-15% среди всех врожденных пороков сердца.
Факторы риска
- Перенесенные в ранних сроках беременности вирусные инфекции,
- скарлатина, коревая краснуха,
- употребление седативных и снотворных препаратов,
- употребление гормональных средств, наркотиков, алкоголя,
- наследственный фактор.
Симптомы
Вся симптоматика обусловлена недостаточным поступлением кислорода в органы и ткани. У новорожденного признаки тетрады Фалло не заметны, так как до рождения этот порок не мешает работе сердца. Через несколько дней или недель после рождения может появиться голубая окраска или синюшность кожи при кормлении грудью, при крике ребенка. У ребенка появляется одышка. С возрастом кожа ребенка принимает синеватый оттенок. Особенно это выражено на губах, ушных раковинах, ногтевых фалангах. .Иногда цианоз проявляется только после того, как ребенок начинает ходить. Из-за нарушения кровоснабжения пальцы больного с возрастом приобретают вид барабанных палочек – утолщаются на конца, ногти приобретают округлую форму в виде «часовых стекол». Дети не могут много двигаться. После нескольких движений они вынуждены присаживаться и отдыхать. Часто больные совсем не встают с постели.
Диагностика тетрады Фалло основывается на внешнем виде больного, прослушивании «сухого», грубого систолического шума слева от грудины.
На электрокардиограмме выявляют признаки гипертрофии правых отделов сердца.
На рентгенограмме видны типичные изменения – сердце в виде «деревянного башмачка».
Помогает диагностике эхокардиография.
Основной метод – это ангиография. Исследование сердца с помощью контрастных веществ. Оно помогает уточнить показания к операции и планировать в каком объеме будет проведена операция.
Лечение.
Тетрада Фалло – это абсолютное показание к оперативному лечению. Если течение порока тяжелое операция на сердце проводится немедленно. Операция проводится в условиях аппарата искусственного кровообращения. Смертности при оперативном лечении у детей раннего возраста не превышает 5%.
Диагностика
- ультразвуковому сканированию сердца,
- зондированию с помощью специального детского эндоскопа,
- выполняется контрастная ангиография.
Лечение
Единственным методом лечения является операция. Обычно оперируют детей, достигших трехлетнего возраста, то есть миновавших опасный период, когда риск операций очень высок. В более ранние сроки или новорожденных оперируют при тяжелой степени порока. Операция выполняется на открытом сердце в условиях искусственного кровообращения и искусственной вентиляции легких. Выполняется ушивание межжелудочкового отверстия, пластика легочной артерии. Нередко хирургам приходится вживлять протез легочного клапана. Для уменьшения объема правого желудочка выполняется частичное удаление фиброзно-мышечного слоя.
Сразу после операции нормализуется кровообращение, у детей исчезают синюшность и одышка.
Прогноз
При выраженной степени стеноза легочной артерии 25% детей умирают на первом году жизни, а 50% не доживают до 5 лет. Только 5% больных могут дожить до 40 лет без оперативного лечения. Причиной смерти в более старшем возрасте обычно бывает сердечная недостаточность.
Минздравовский порядок организации проведения обследования новорожденных детей на наследственные заболевания
На федеральном уровне Положение об организации проведения массового обследования новорожденных детей на наследственные заболевания установлено Приказом Минздравсоцразвития РФ от 22.03.2006 № 185 (далее – Положение № 185).
Положение № 185 регулирует вопросы организации проведения в государственных и муниципальных учреждениях здравоохранения массового обследования новорожденных детей (далее – неонатальный скрининг) на наследственные заболевания (адреногенитальный синдром, галактоземию, врожденный гипотиреоз, муковисцидоз, фенилкетонурию).
Пунктом 2 Положения № 185 определено, что для проведения неонатального скрининга производится забор образцов крови специально подготовленным работником у новорожденных детей в государственных и муниципальных учреждениях здравоохранения, оказывающих медицинскую помощь женщинам в период родов.
Одновременно с этим, пунктом 15 Порядка оказания медицинской помощи по профилю «неонатология» (Приказ Минздрава России от 15.11.2012 № 921н) установлена норма о внесении данных неонатального скрининга в медицинскую документацию новорожденного.
При этом, Приказом Минздравсоцразвития РФ от 22.03.2006 № 185 установлены также и Рекомендации по забору образцов крови при проведении массового обследования новорожденных детей на наследственные заболевания, пунктом 2 которых определено, что в случае отсутствия в документации новорожденного ребенка отметки о заборе образца крови при его поступлении под наблюдение в детскую поликлинику по месту жительства или переводе по медицинским показаниям в больничное учреждение, забор образца крови для проведения исследования осуществляется специально подготовленным работником.
Пунктом 3 указанных Рекомендаций определено, что образец крови берут из пятки новорожденного ребенка через 3 часа после кормления на 4 день жизни у доношенного и на 7 день – у недоношенного ребенка, а также поэтапно описывается процесс забора крови.
Эндоваскулярный (внутрисосудистый) метод закрытия ДМПП
Схема имплантацииокклюдера
Эндоваскулярный (внутрисосудистый) метод закрытия дефекта межпредсердной пререгородки (ДМПП) начал развиваться с 1975 года. Устройство для эндоваскулярного закрытия дефекта получило название окклюдер. В последующие годы было испытано несколько поколений окклюдеров, но только с 2001 года устройства получили международное одобрение для использования в повседневной медицинской практике.
Современные окклюдеры обладают необходимыми качествами для использования:
- имеют легкую и удобную систему доставки непосредственно к дефекту,
- полностью выполняют отверстие дефекта,
- обладают способностью к репозиционированию и извлечению в сложных анатомических случаях.
Этапы эндоваскулярной имплантации окклюдера ДМПП
В мировой медицинской практике эндоваскулярное закрытие ДМПП стало операцией выбора, то есть первоочерёдным и оптимальным методом лечения. Закрытие вторичного ДМПП с помощью эндоваскулярной технологии с использованием окклюдера возможно в 80% случаев. Возможность эндоваскулярного метода лечения определяется анатомо-морфологическими характеристиками дефекта.
Преимущества методики:
- отсутствие разрезов и швов на теле;
- проведение операции через прокол бедренной вены;
- без наркоза, под местным обезболиванием;
- отсутствие длительной реабилитации после проведения операции;
- возможность вернуться к повседневной жизни через несколько дней после операции.
Для определения возможности выполнения операции эндоваскулярного закрытия ДМПП проводится трансторакальное Эхо-Кг и чреспищеводное Эхо-Кг.
После оценки показателей данных исследований принимается решение об анатомической и морфологичсекой возможности выполнения операции.
Виды пороков сердца
В большинстве случаев, пороки сердца поражают клапанный аппарат. Появившиеся в результате этой патологии осложнения могут стать причиной ранней потери трудоспособности и даже смерти.
Основная роль клапанного аппарата – свободно пропускать кровь через себя при сокращении сердца и задерживать обратное движение крови через клапан при расслаблении, сохраняя ритмичный и непрерывный поток крови. Дефектные клапаны перестают полноценно выполнять эту работу и функции, из-за чего кровь с трудом поступает через суженный клапан в полость сердца и в полной мере не покидает камеры или поступает обратно через закрытый клапан.
Приобретенные пороки сердца:
- недостаточность клапана (неполное смыкание створок или повреждение створок) – вызывает обратный ток крови;
- стеноз клапана (сужение просвета между открытыми створками) – затрудняет кровообращение;
- пролабирование (выпячивание) клапана, в результате чего его створки выбухают в сердечную полость, и часто происходит обратный ток крови вследствие недозакрытия клапана.
В кардиологической практике часто встречаются комбинированные и сочетанные пороки, при которых поражены сразу несколько клапанов.
Чаще всего от аномальных изменений страдают митральный (митральный порок сердца) и аортальный (аортальный порок сердца) клапаны сердца.
Врожденные пороки сердца:
- дефект межпредсердной перегородки;
- дефект межжелудочковой перегородки;
- открытый артериальный проток;
- транспозиция (нарушение положения) крупных магистральных сосудов;
- коарктация аорты;
- стеноз легочной артерии и др.
Врожденные пороки сердца могут встречаться как по отдельности, так и в комбинациях друг с другом. Так, сочетание гипертрофии правого желудочка, транспозиции аорты, дефекта межжелудочковой перегородки и стеноза выходного тракта правого желудочка носит название тетрады Фалло (или синего порока сердца).
1
Рентгенография при пороках сердца
2
Диагностика пороков сердца с помощью рентгена
3
УЗИ при пороках сердца
Открытый артериальный проток
Что такое открытый артериальный проток (боталлов проток)?
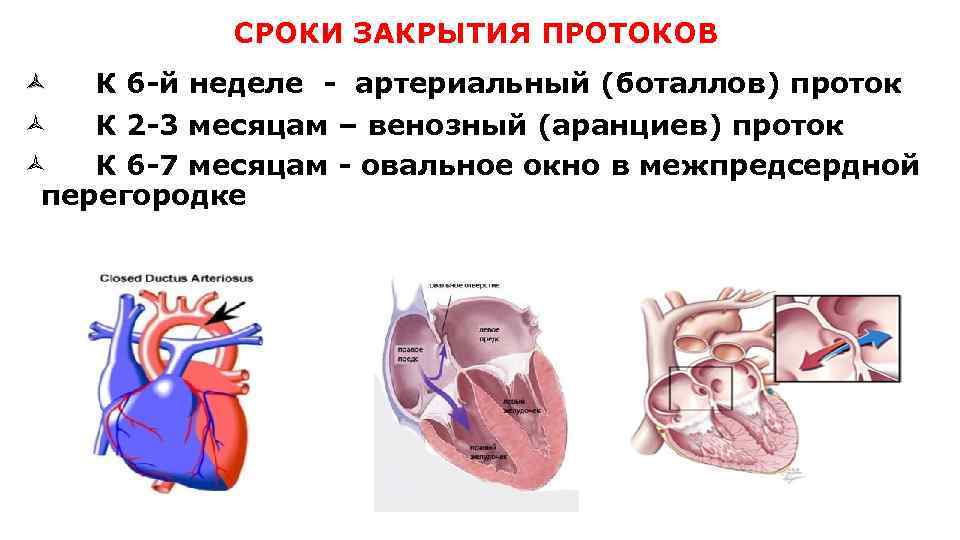
Боталлов проток (Рис 1, Видео 1) – это сосуд, который в норме функционирует у плода и соединяет два магистральных сосуда сердца – аорту и легочную артерию. Существует он для того, что бы кровь могла обойти мимо легкие, которые у внутриутробно не функционируют. В течение первых дней жизни новорожденного малыша боталлов проток в норме закрывается. Иногда случается, что открытый артериальный проток не закрывается, что приводит к ряду неприятных проблем. Проток, который не закрылся в течение месяца жизни ребенка, считается врожденным пороком сердца.
Естественное течение порока. Или к чему приведет открытый боталов проток?
Дело в том, что этот сосуд все еще соединяет два больших сосуда сердца – аорту и легочную артерию. Давление в аорте намного превышает давление в легочной артерии. Поэтому через открытый артериальный проток с аорты в легкие попадает избыточное количество крови, что сначала приведет к частым бронхолегочным заболеваниям, а при очень больших боталловых протоках – к необратимым изменениям в сосудах легких и неоперабельности. Кроме того, большой боталлов проток значительно увеличивает нагрузку на сердце, особенно на левый желудочек. Поэтому затягивать с лечением этого порока нельзя.
Лечение открытого артериального протока.
В настоящее время не существует такого боталлова протока, который нельзя было бы закрыть нетравматичным эндоваскулярным методом, который позволит избежать разреза, шрамов и длительной реабилитации. Хирургическое лечение этого порока осталось в прошлом, хирурги закрывают боталлов проток только недоношенным детям или в странах, где медицина имеет недостаточное финансирование. Во всех развитых странах Европы и Америки этот порок устраняется исключительно эндоваскулярно в ренгеноперационных. К тому же вероятность осложнений при эндоваскулярном лечении намного меньше.
Процедура эндоваскулярного закрытия.
Рис 2 – Внешний вид окклюдера |
Рис 3 – Внешний вид спирали |
При эндоваскулярном закрытии через маленький прокол в бедренные сосуды в сосуды сердца и в боталлов проток заводятся тоненькие трубочки, так называемые катетеры. Используя рентген и контрастное вещество, доктор оценивает размер и форму боталлова протока, после чего он выбирает самое подходящее окклюзирующее (от англ. Occlusion – закупорка) устройство. В качестве таких устройств могут использоваться окклюдеры (рис 2; Видео 1, 2, 3) или спирали (рис 3; Видео 4, 5, 6).
Выбор устройства для закрытия происходит во время операции, и зависит от размера и формы боталлова протока. Как правило, для больших протоков используются окклюдеры, для маленьких – спирали. В течение полугода окклюзирующие устройства полностью обрастают собственными клеточками сердца, происходит, так называемая, эндотелизация. Сброс через боталлов проток в 90% случаев прекращается сразу же после процедуры, в остальных случаях – по окончанию периода эндотелизации устройства.
Реабилитация после процедуры
1. Пациентов выписывают, как правило, на следующий день после процедуры. 2. В течении 6 месяцев рекомендуется проводить антибиотикопрофилактику инфекционного эндокардита.
У нас наибольший в Украине опыт по эндоваскулярному лечению открытых артериальных протоков – более 300 операций. Мы имеем доступ к оборудованию для закрытия боталлового протока любого размера и формы. Также, специализируемся на лечении дефектов межпредсердной и межжелудочковой перегородок. Для того чтобы попасть к нам на консультацию или госпитализироваться позвоните по одному из телефонов или запишитесь на прием онлайн.
Видео 1 – Боталлов проток |
Видео 2 – В этой красочной анимации Вы сможете увидеть, как закрывают боталлов проток окклюдером |
Видео 3 – Видео из операционной: кровь через открытый боталлов проток (сосуд по центру) попадает из аорты (крупный сосуд справа) в легочную артерию (сосуд слева) |
Видео 4 – Видео из операционной: проток перекрыт окклюдером. Сброс крови прекратился |
Видео 5 – А в этом видео Вы сможете увидеть, как закрывают боталлов проток спиралью |
Видео 6 – Видео из операционной: кровь через открытый боталлов проток (сосуд по центру) попадает из аорты (крупный сосуд справа) в легочную артерию (сосуд слева) |
Видео 7 – Видео из операционной: проток перекрыт спиралью. Сброс крови практически прекратился |
Общая информация
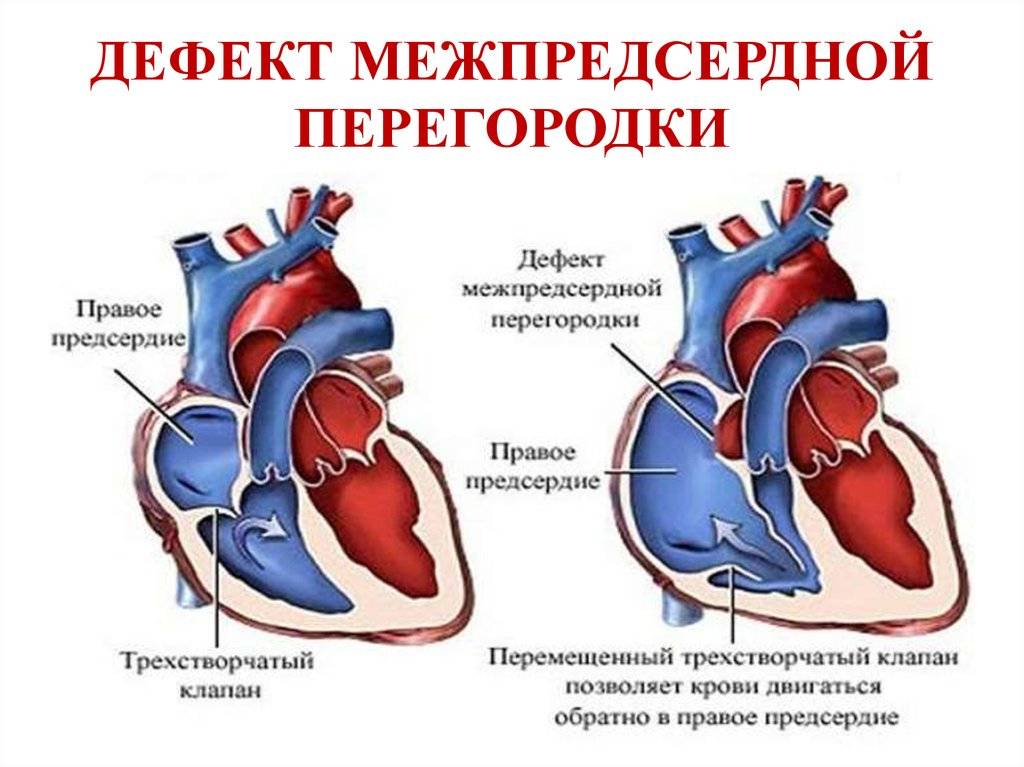
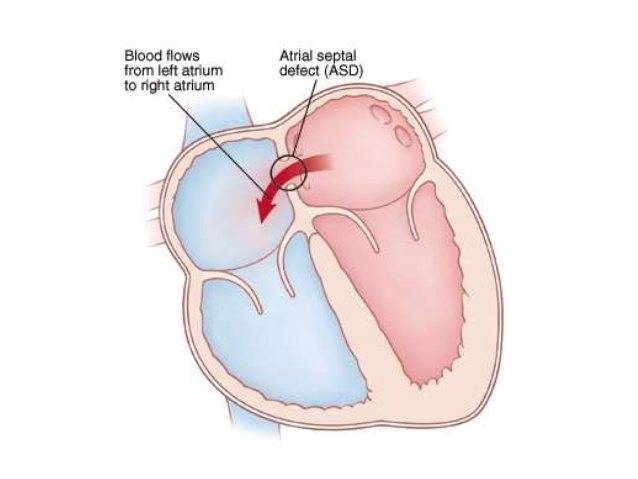
Дефект межпредсердной пререгородки (ДМПП) — самый часто встречающийся врожденный порок сердца у взрослых, находится на втором месте по частоте развития у детей.
 Дефект межпредсердной пререгородки (ДМПП)
Дефект межпредсердной пререгородки (ДМПП)
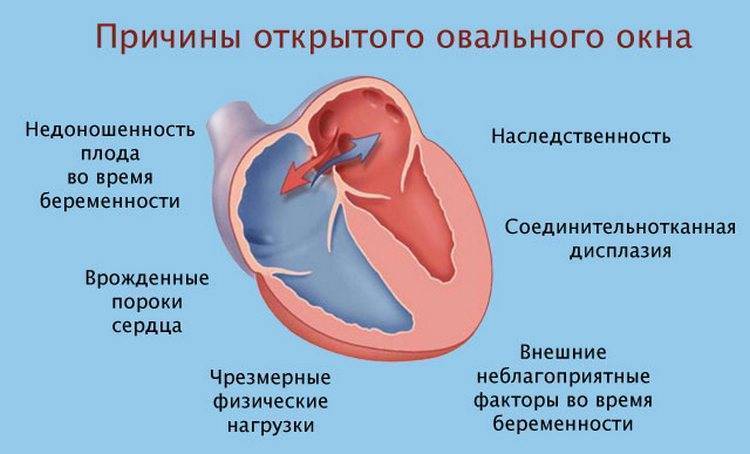
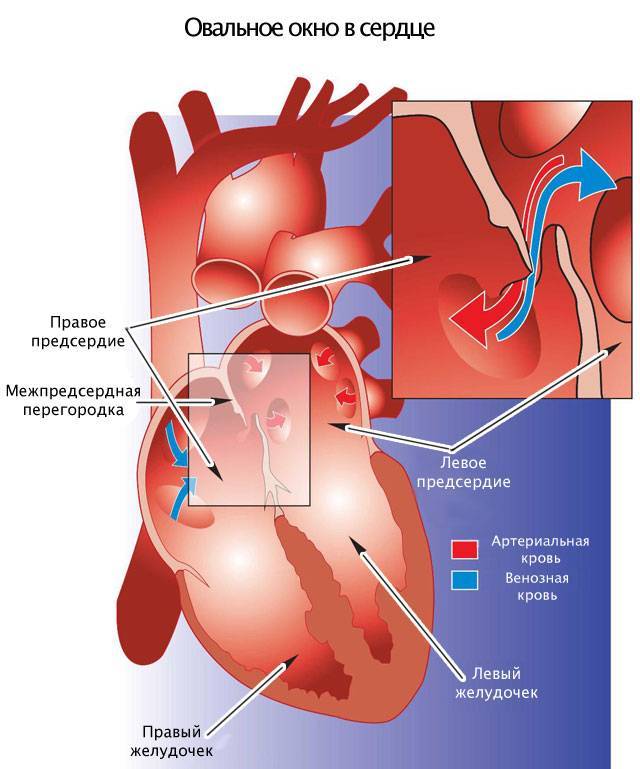
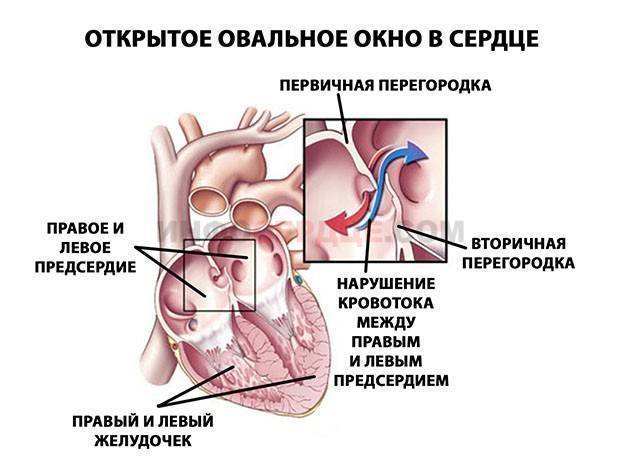
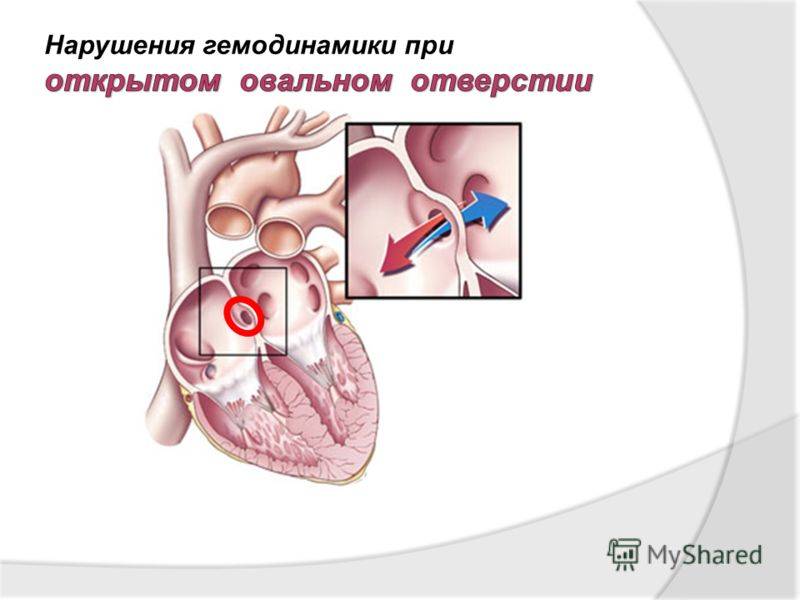
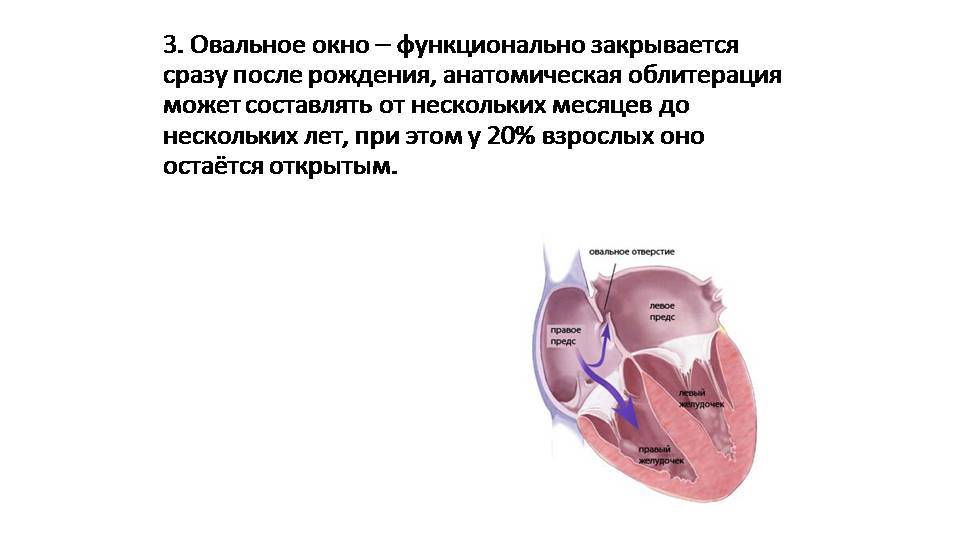
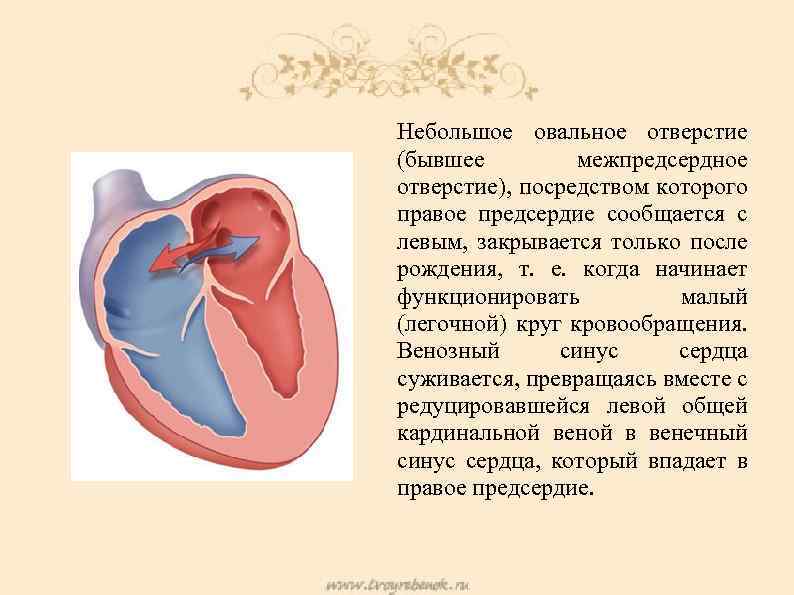
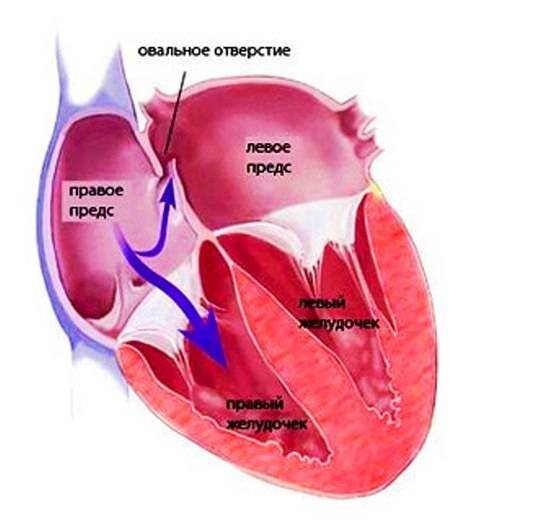
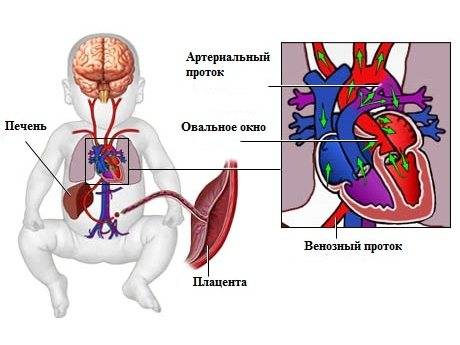
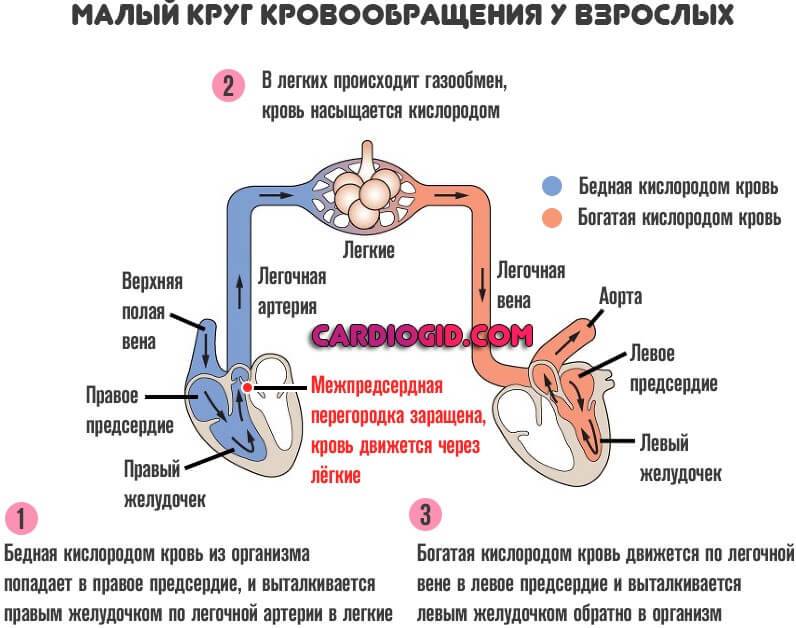
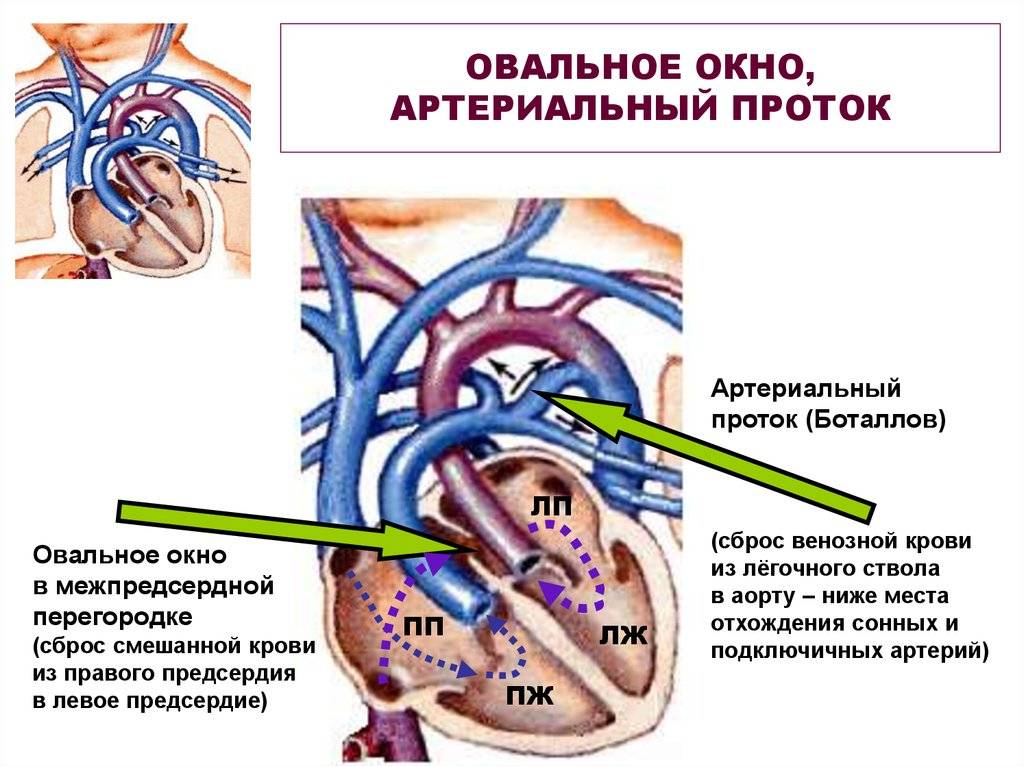
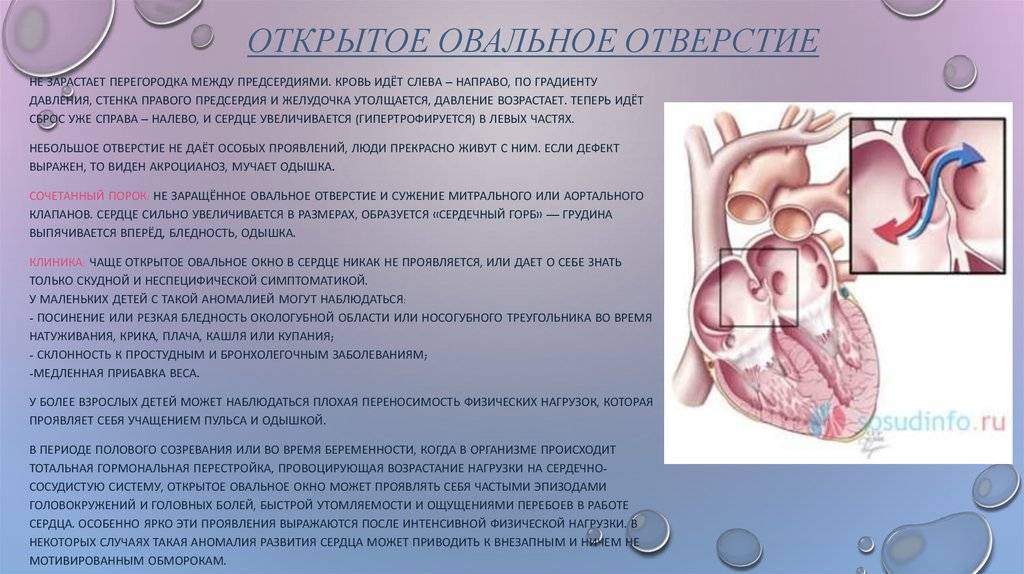
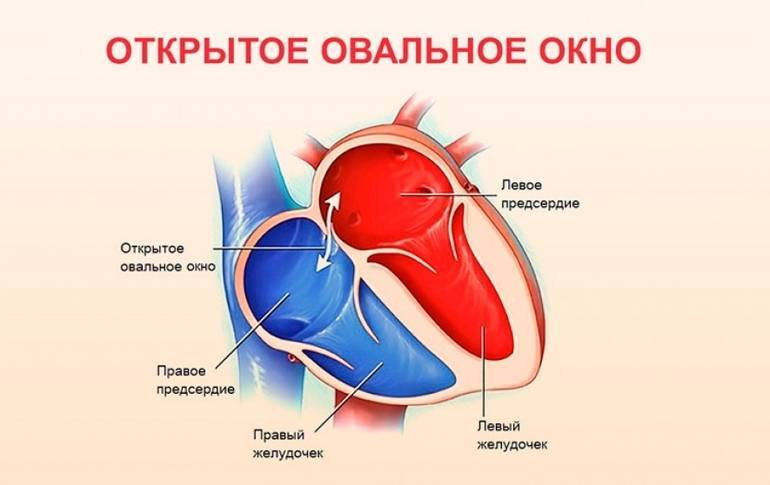
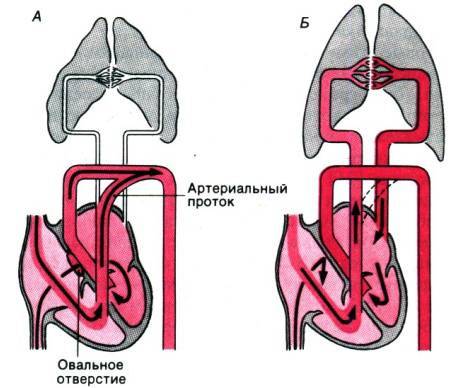
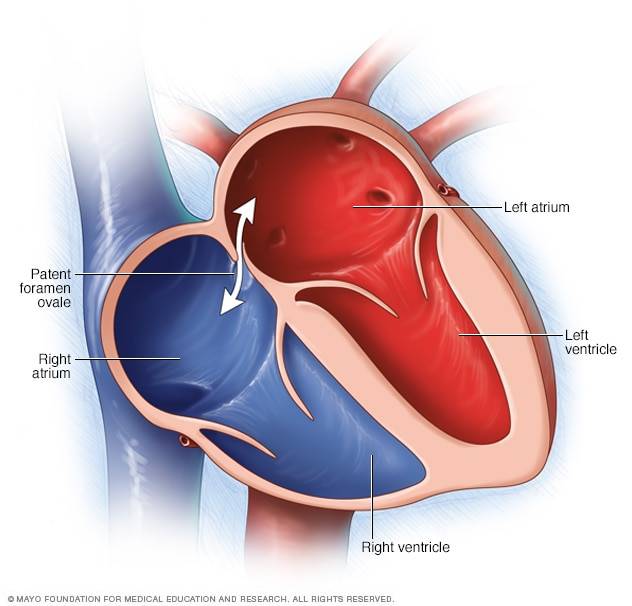
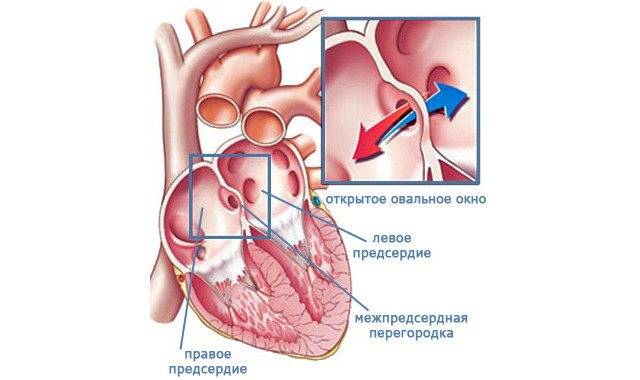
Деление единого общего предсердия на две части, правую и левую, начинается уже к пятой неделе развития плода внутри утробы матери. В последующем начинает появляться межпредсердная перегородка, которая развивается из двух частей. Сначала — первичная перегородка, а затем — вторичная перегородка. Перегородки располагаются параллельно и плотно друг к другу. До рождения между предсердиями функционирует физиологическое сообщение — щель между первичной и вторичной перегородками, прикрытая гибкой створкой — это так называемое «овальное окно».
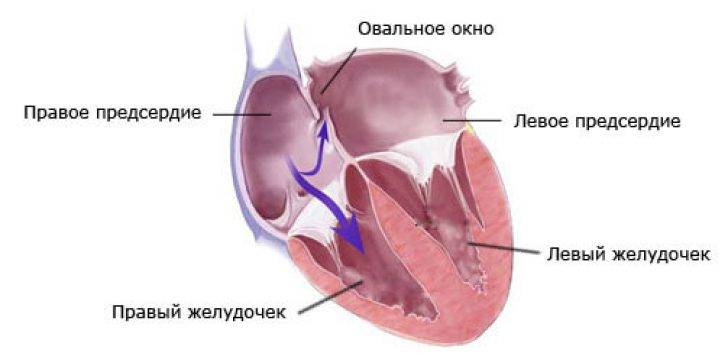
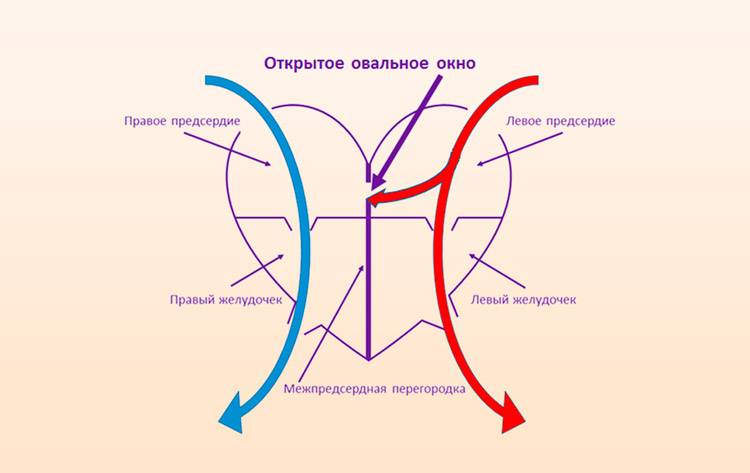
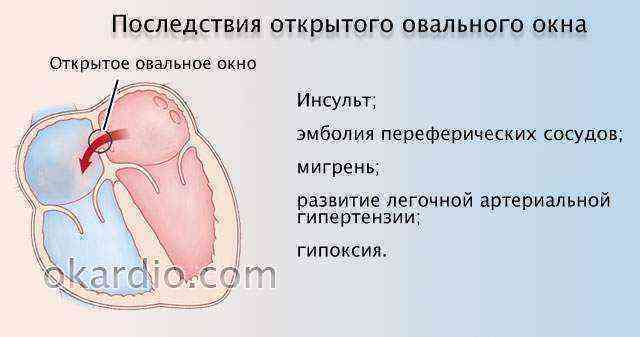
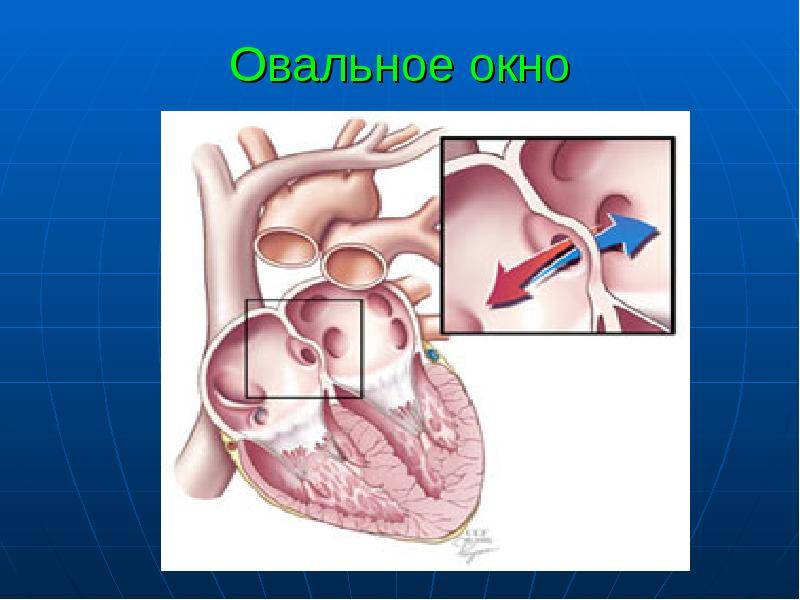
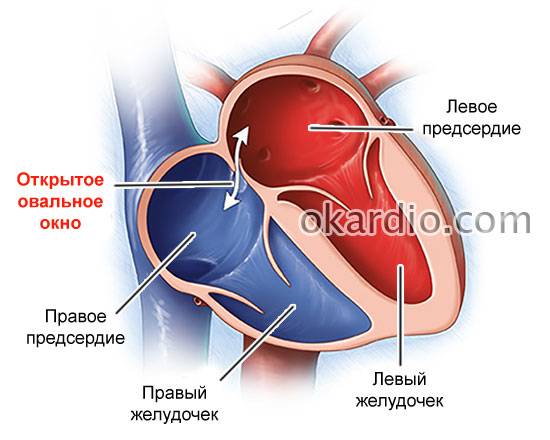
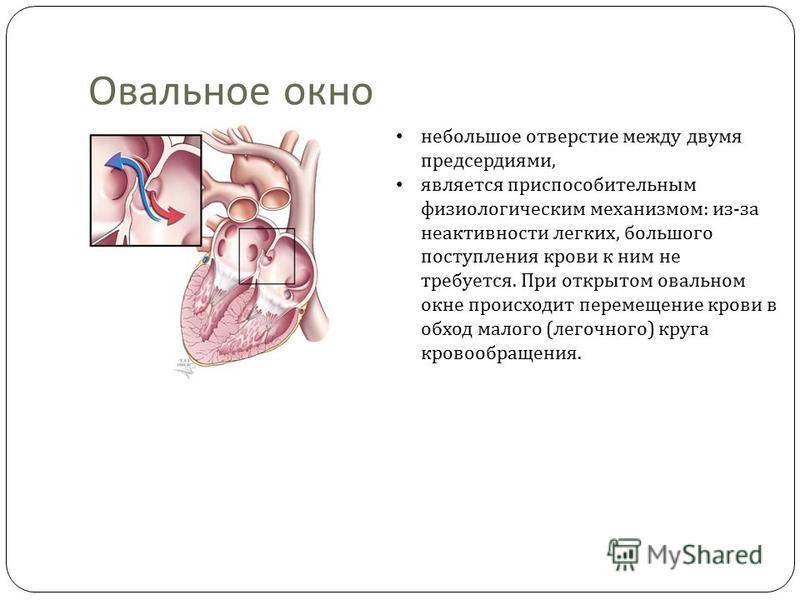
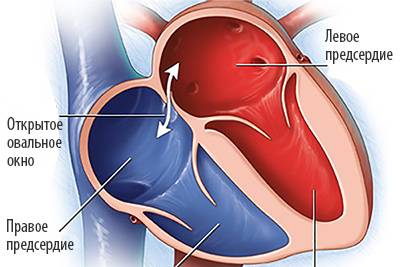 Овальное окно
Овальное окно
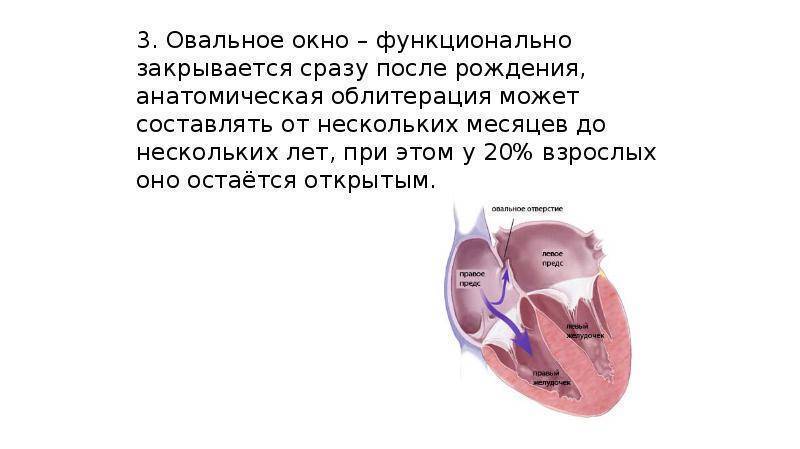
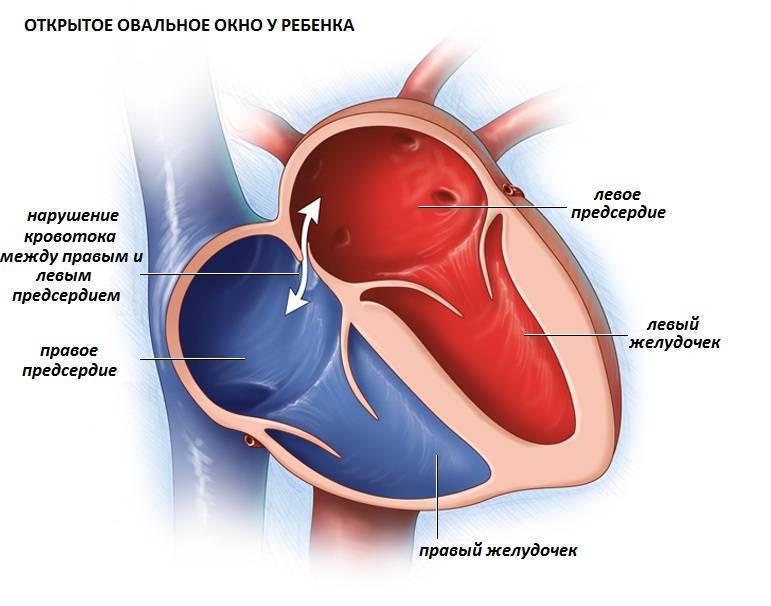
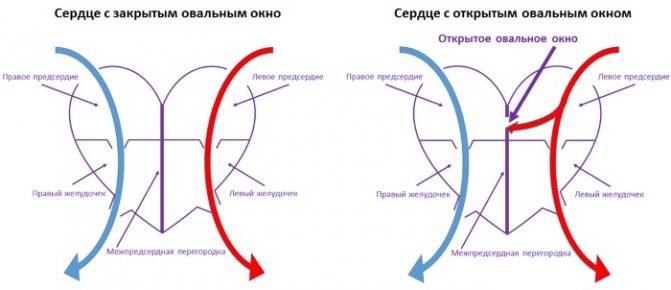
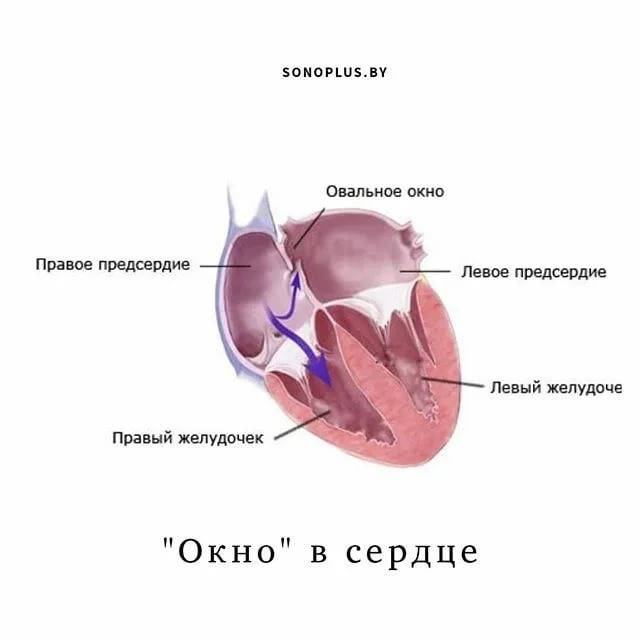
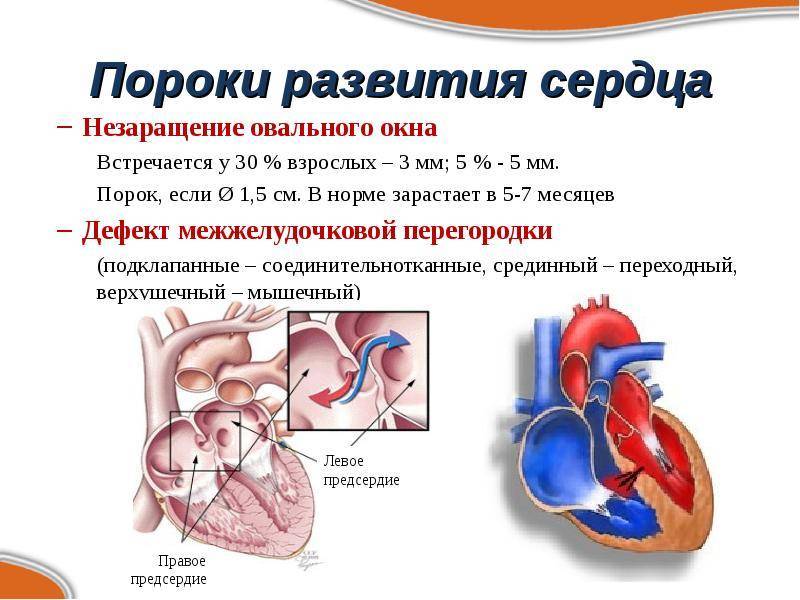
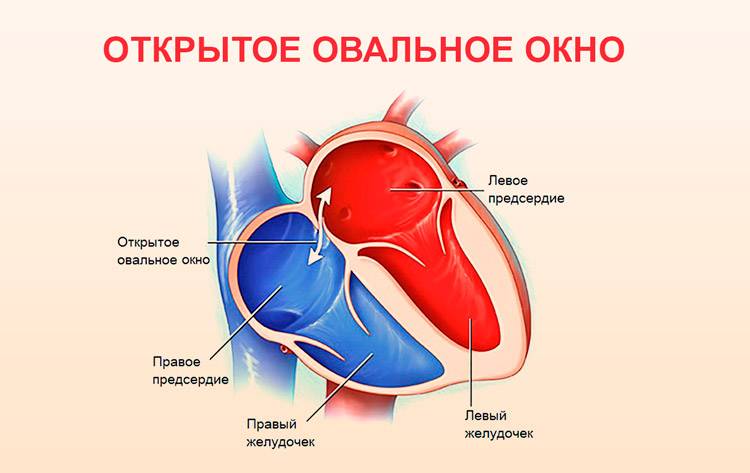
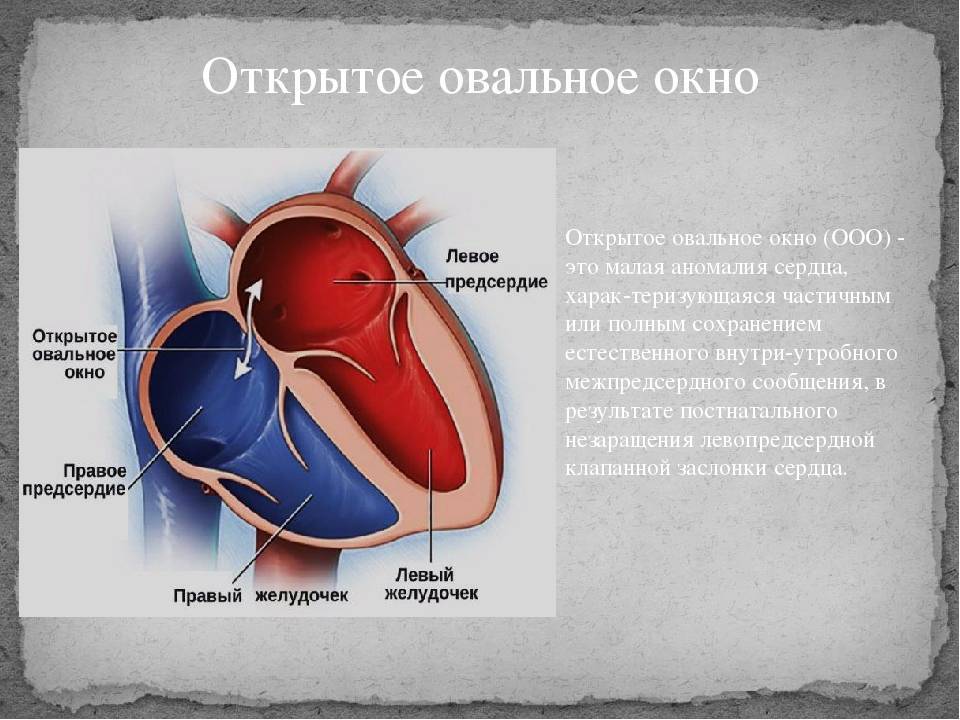
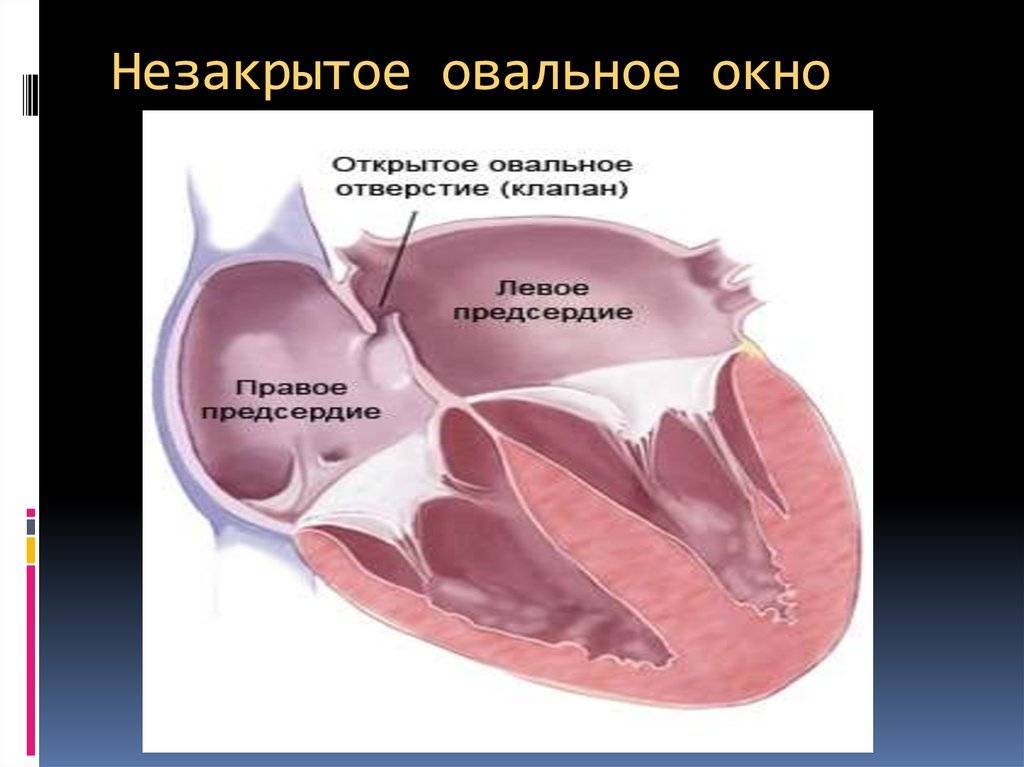
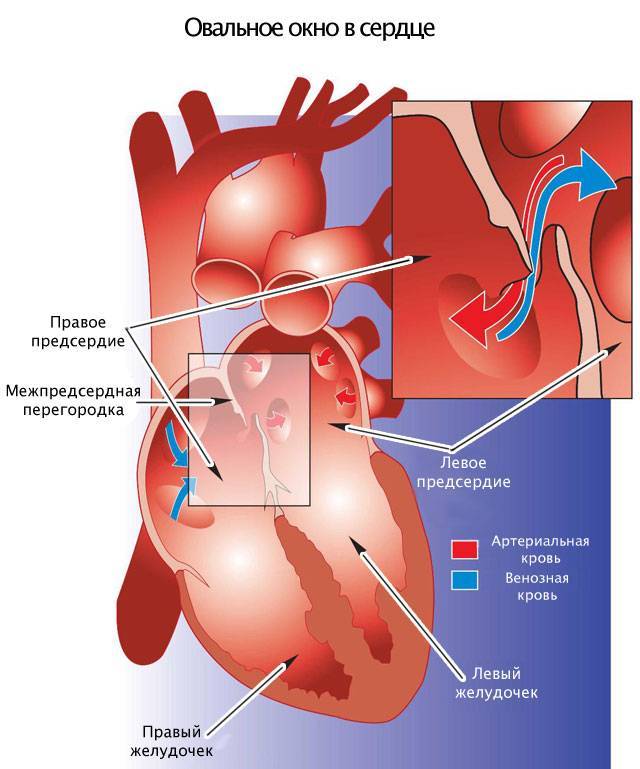
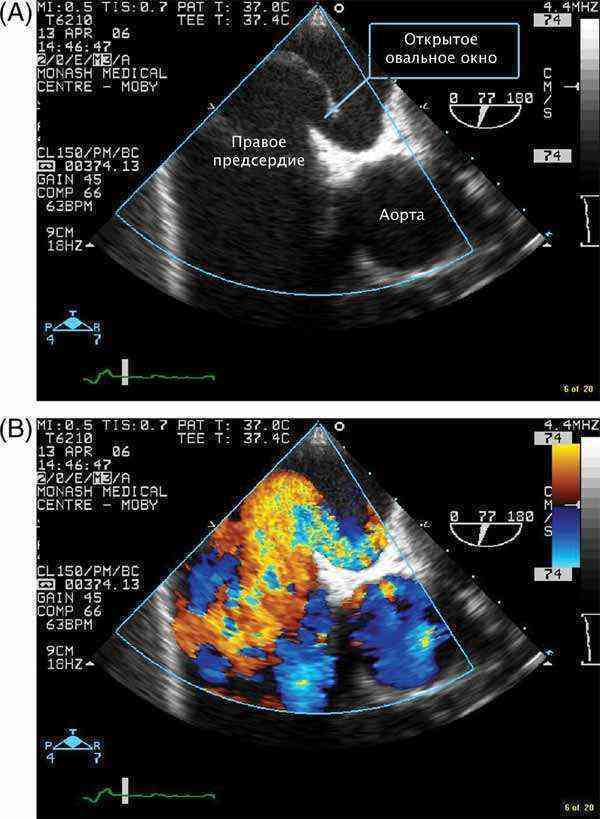
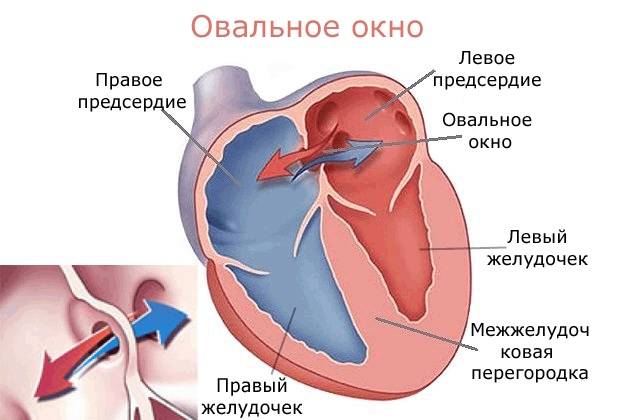
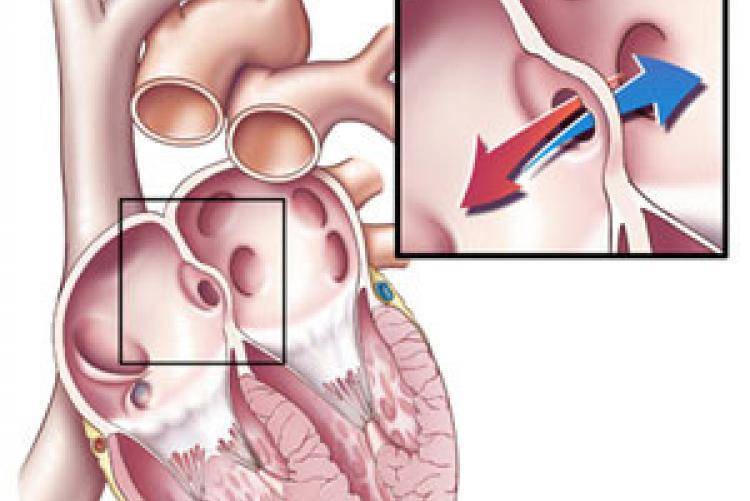
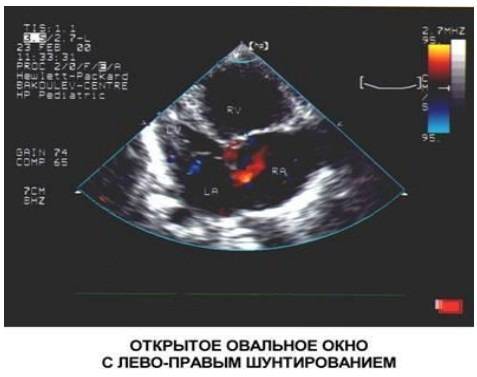
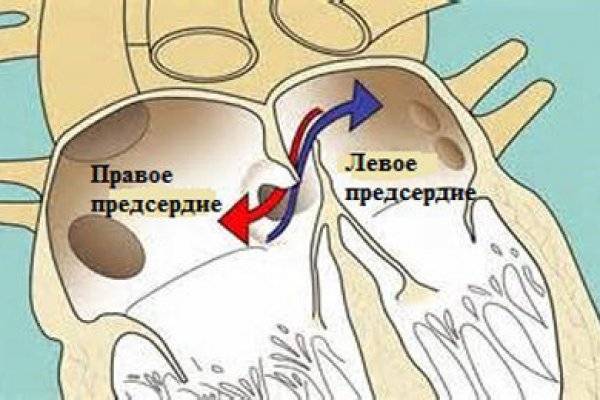
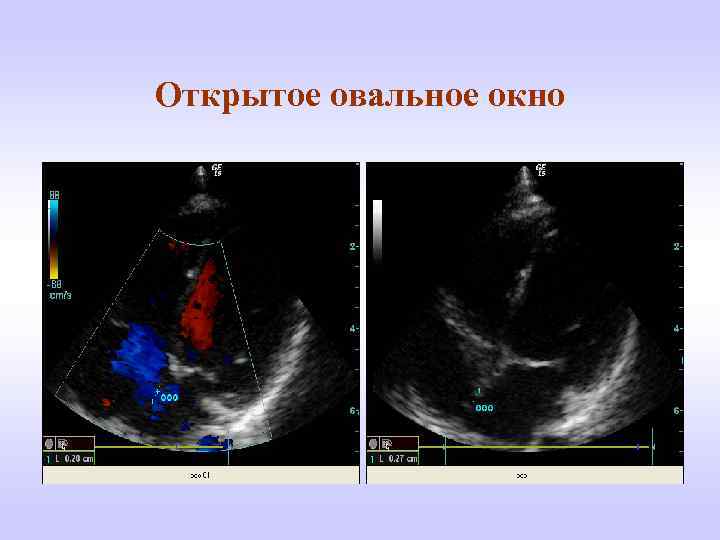
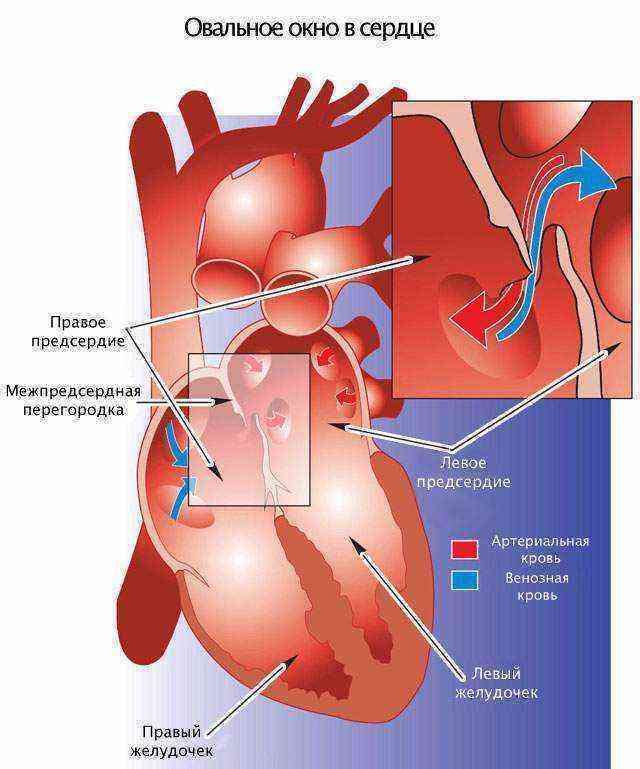
Проходимость «овального окна» осуществляется вследствие того, что давление в правом предсердии выше и кровь из правого предсердия попадает в левое. Сообщение между предсердиями необходимо, так как у плода не функционируют легкие. После рождения, когда новорожденный начинает дышать, давление в правом предсердии падает и гибкая створка закрывает щель между предсердиями, это происходит в 70% случаев. В 30% «случаев овальное» окно остаётся открытым и в подавляющем большинстве случаев закрывается в течение двух лет после рождения. В редких случаях открытое «овальное окно» может сохраняться в течение всей жизни, обычно не влияет на работу сердца и крайне редко нуждается в закрытии.
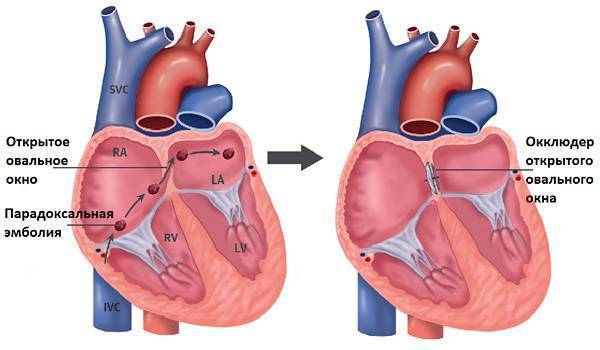
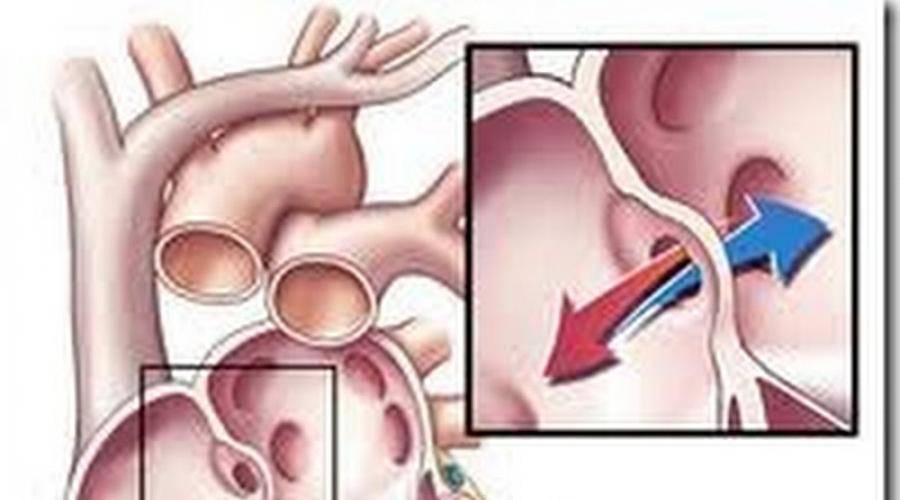
 Овальное окно и закрытие его с помощью окклюдера
Овальное окно и закрытие его с помощью окклюдера