Что такое HIPEC
Суть методики HIPEC — в том, что сразу после циторедуктивной (т. е. направленной на удаление опухолевых клеток) операции на брюшине и органах брюшной полости, пациенту в течение 60–90 минут проводят перфузию — «промывают» брюшную полость концентрированным раствором химиопрепарата, нагретым до 42–43 °C.
Цель — уничтожить максимум опухолевых клеток, которые неизбежно останутся даже после самого тщательного хирургического удаления очагов и спровоцируют рецидив.
Свойства, которые делают HIPEC действительно уникальной методикой, мы разъясним чуть ниже, а сначала определимся, при каких диагнозах она может помочь и почему она иногда оказывается единственным способом продлить жизнь человеку на последних стадиях рака.При каких опухолях образуется канцероматоз брюшины, и почему он так опасен
В брюшную полость распространяются многие из часто встречающихся видов рака.
- рак яичников — в 60–70% случаев приводит к канцероматозу;
- рак желудка — канцероматоз в 40–50% случаев;
- рак поджелудочной железы — в 30–40% случаев;
- рак толстой и прямой кишки (колоректальный рак) — в 10–15% случаев;
- рак печени;
- рак шейки матки;
- рак червеобразного отростка (аппендикса);
- редкие первичные опухоли брюшины (мезотелиома и псевдомиксома).
Все эти злокачественные новообразования распространяют раковые клетки либо когда первичная опухоль физически прорастает в брюшную полость, либо вместе с током крови и лимфы — иногда это происходит во время хирургических операций по поводу первичных опухолей.
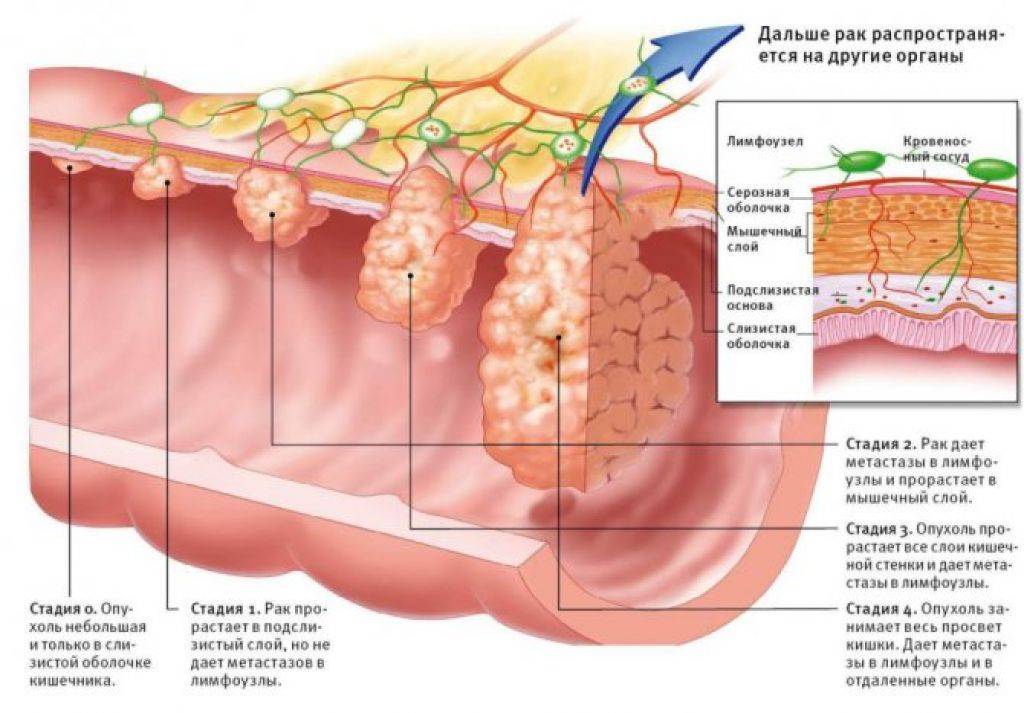
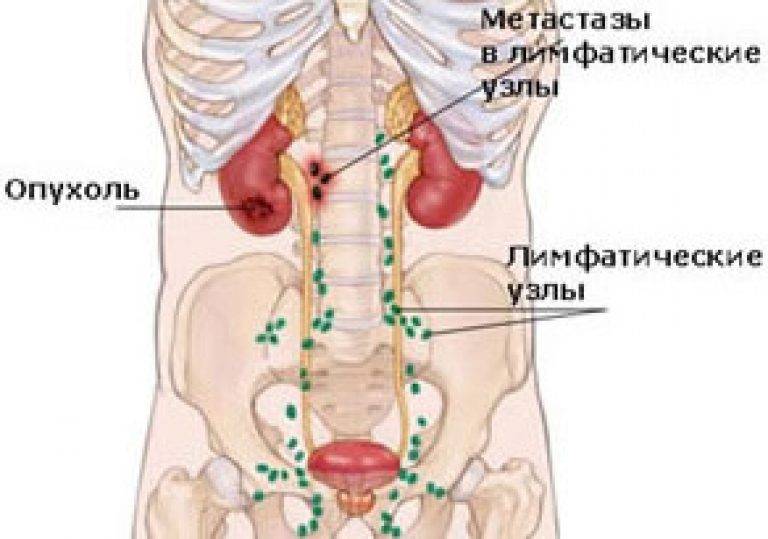
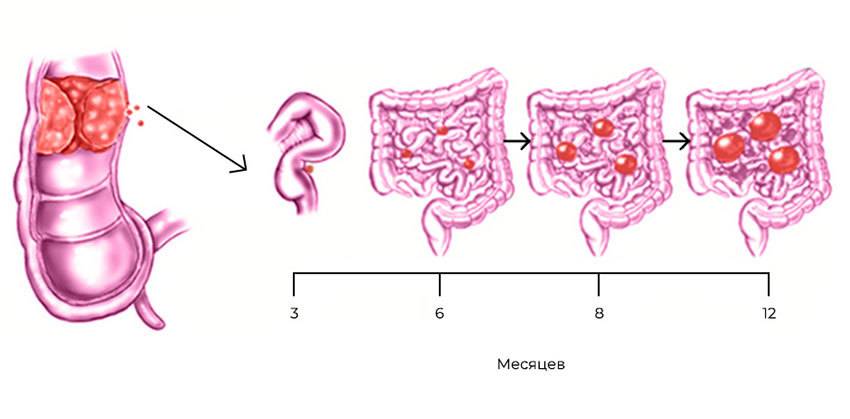 Развитие канцероматоза при колоректальном раке: из прямой кишки в брюшную полость
Развитие канцероматоза при колоректальном раке: из прямой кишки в брюшную полость
Стоит раковым клеткам попасть в полость, ограниченную брюшиной — они, скорее всего, дадут начало вторичным опухолям, метастазам. Перитонеальная ткань — богатый источник факторов роста и комфортная среда для их развития. Микроскопические метастазы распространяются по поверхности брюшины, поражают внутренние органы.
Метастазы нарушают кровоток и лимфоток, лишают внутренние органы питания и пространства, зачастую становятся причиной непроходимостей (например, кишечной, или сдавливают мочеточники). Кроме того, это провоцирует асцит — выпот и скопление жидкости в брюшной полости — наиболее распространенный симптом при канцероматозе.
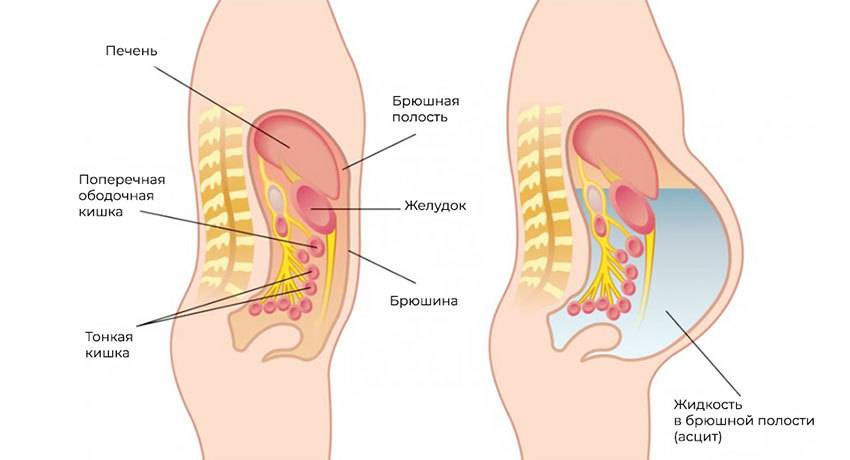 Асцит — скопление жидкости в брюшной полости
Асцит — скопление жидкости в брюшной полости
Застой крови и лимфы, интоксикация, сдавление внутренних органов метастазами и/или скопившейся жидкостью при асците — это причины, почему пациенты с канцероматозом без лечения не проживают и года.
Другие методы лечения в таких случаях — не работают
На протяжении почти всей истории онкологии считалось, что перитонеальный карциноматоз и опухоли брюшины не поддаются никакому из существующих видов лечения.
Лучевая терапия в лечении канцероматоза не применяется, поскольку высокие дозы облучения такой обширной области живота опасны для пациента еще более серьезными осложнениями.Хирургическое лечение малоэффективно, т. к. метастазы на поверхности брюшины могут быть микроскопического размера, либо расположены в недоступных местах, и врач не видит их во время операции. А для быстрого рецидива канцероматоза достаточно и единичных раковых клеток, оставшихся в полости брюшины.
Системная химиотерапия почти не дает чувствительного воздействия на опухоли брюшины -опухолевые очаги размером до 3 мм (таких при канцероматозе большинство) практически не развивают систему собственных кровеносных сосудов — и поэтому слабо доступны для системной внутривенной химиотерапии.
Вводить химиотерапию в более высоких дозах, чтобы повысить концентрацию препаратов в перитонеальной области — невозможно, т. к. это может необратимо навредить остальным органам и тканям, до которых доберется перенасыщенный химиопрепаратом кровоток.
Поэтому долгое время считалось, что пациенты с карциноматозом брюшины — неизлечимы. И до сих пор многие врачи — кстати, в разных странах — придерживаются того же мнения. Среди наших пациентов часто бывают те, кого «выписали» из больницы, потому что «канцероматоз нечем лечить». Когда они приходят к нам и узнают про возможность лечения с помощью HIPEC — оказывается, что о такой методике они слышат впервые.
Во второй половине 20 века появились первые работы, рассказывающие о возможностях применения внутрибрюшинной химиотерапии. Последние 20 лет это направление активно развивается, а создал его еще в 80-х годах XX века американский хирург-онколог Пол Шугабейкер — он первым придумал совместить циторедуктивную операцию с горячей химиотерапией, вводимой непосредственно в брюшную полость. И это дало результат
Как все происходит
Процедура HIPEC — это, строго говоря, вторая половина целого комплекса мероприятий. Без циторедуктивной хирургической операции HIPEC может проводиться в считанном количестве случаев по особым показаниям. Обычно, процедура — продолжение хирургической операции, которое дает серьезное улучшение прогноза выживаемости.
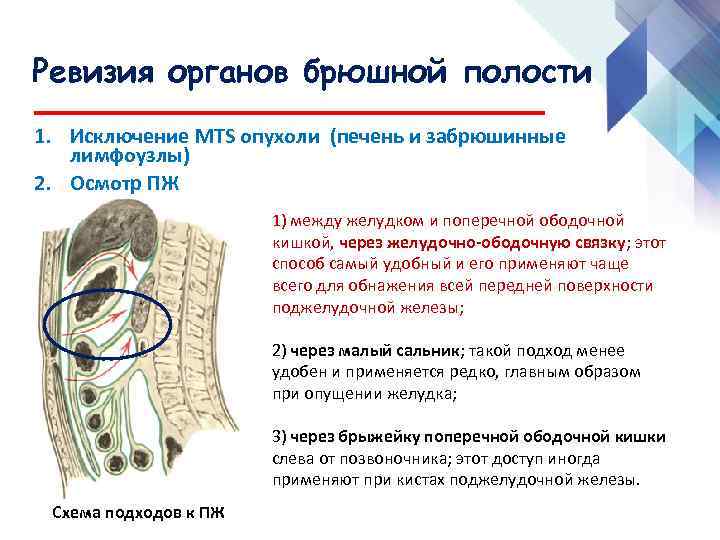
Вместе с удалением опухолевых очагов, все вмешательство занимает от 6 до 18 часов. Процесс можно разделить на 4 этапа.
1) Ревизия брюшной полости. Проводится она для того, чтобы понять, показано ли лечение с помощью HIPEC для этого пациента, принесет ли оно увеличение продолжительности жизни и улучшение ее качества. Во время ревизии хирург внимательно осматривает брюшную полость и определяет перитонеальный индекс рака (peritoneal cancer index — PCI).
Чтобы его рассчитать, брюшную полость и тонкую кишку условно делят на 13 областей-квадрантов, в каждом из них оценивают самый крупный опухолевый очаг по шкале от 0 до 3:
- очагов не обнаружено — 0 баллов;
- очаги размером менее 0,5 см — 1 балл;
- очаги размером менее 0,5–5 см — 2 балла;
- очаг более 5 см или несколько узлов меньшего размера- 3 балла.
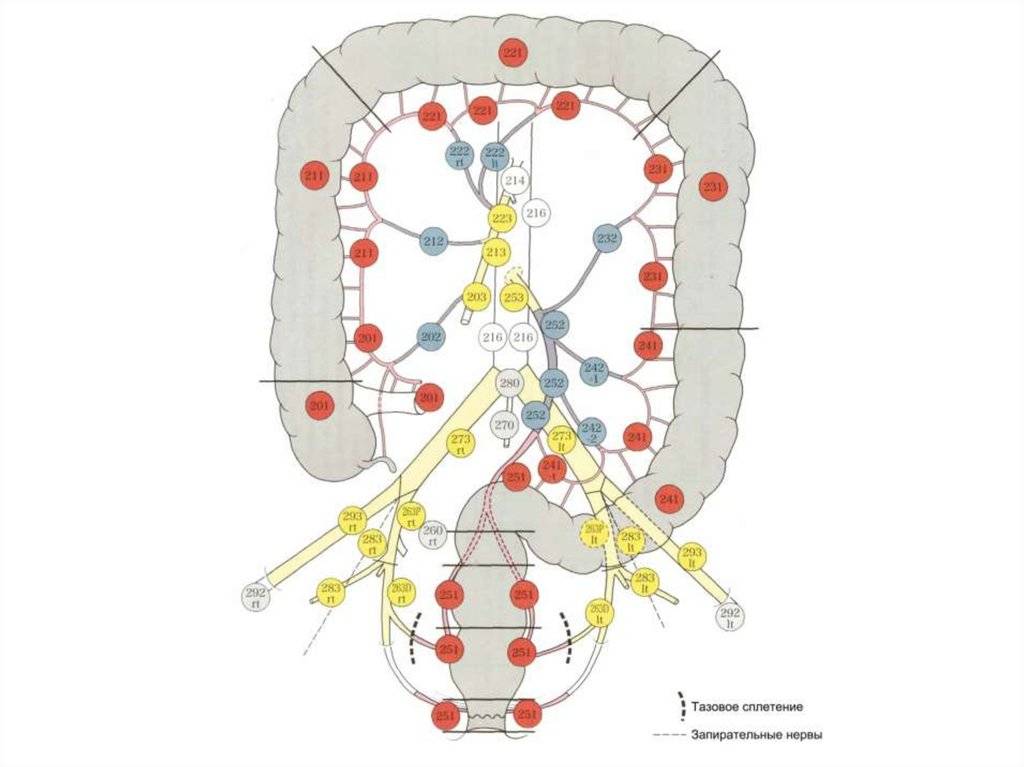
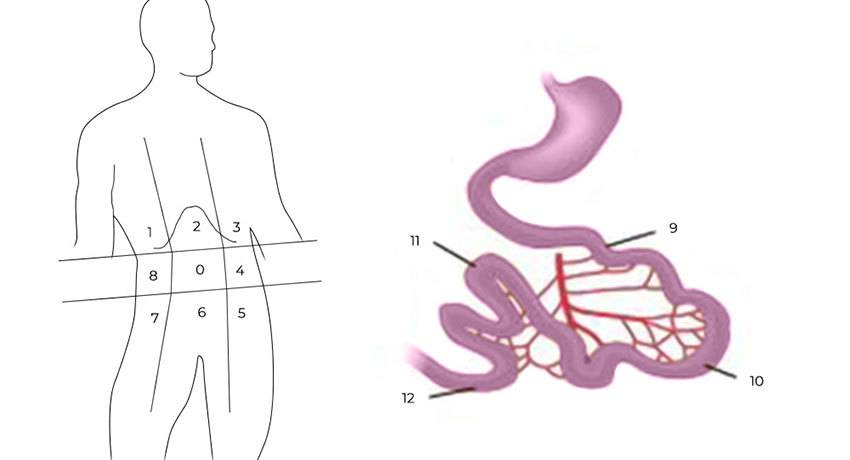 Разделение брюшной полости на участки для определения PCI
Разделение брюшной полости на участки для определения PCI
Баллы суммируются по всем квадрантам — это и есть значение PCI. Чем больше баллов — тем хуже прогноз
Если PCI выше критического (принимая во внимание тип опухоли и состояние пациента) — то и операцию, и процедуру HIPEC могут признать нецелесообразными
Проводят ревизию интраоперационно, т. е. непосредственно перед проведением основной операции. В некоторых случаях ее можно провести в виде отдельной диагностической лапароскопической операции — малотравматичной, через небольшие проколы в стенке живота.
2) Циторедуктивная операция. Если по результатам ревизии PCI оценен как удовлетворительный, то хирург приступает к удалению всех видимых и пальпируемых (те, что чувствуются наощупь) опухолевых узлов.
Удаляют отдельные участки брюшины, орган, в котором находится первичная опухоль, соседние внутренние органы или их части, если они тоже поражены метастазами. Часто это участки кишечника, селезенка, желчный пузырь.
У нас в «Медицине 24/7» хирурги могут провести у стола на этом этапе и 6, и 9 часов, потому что понимают — от того, как тщательно они выполнят свою работу, зависит то, как эффективно будет и дальнейшая процедура HIPEC. А значит и то, насколько дольше проживет пациент.
3) Гипертермическая интраперитонеальная химиотерапия. Собственно, HIPEC. В брюшную полость вводят катетеры и температурные датчики, соединенные со специальным аппаратом и емкостью с раствором химиопрепарата. Эта перфузионная система (под контролем врачей, конечно) поддерживает заданную температуру и давление циркулирующей жидкости. Раствор химиопрепарата в течение 60–90 минут циркулирует в брюшной полости пациента.
За это время он и чисто механически «вымывает» все сгустки крови и лимфы, на которых опухолевые клетки могли закрепиться. Горячий химиотерапевтический препарат глубоко действует на ткани, где могли остаться невидимые для хирурга микро-метастазы и уничтожает эти зарождающиеся опухоли до того, как они успеют развиться. Кроме того, химиопрепарат активно проникает в лимфоузлы, которых множество в брюшной полости, что препятствует дальнейшему распространению метастазов по организму.
После процедуры препарат удаляют из брюшной полости, промывают ее физраствором, удаляют датчики и катетеры.
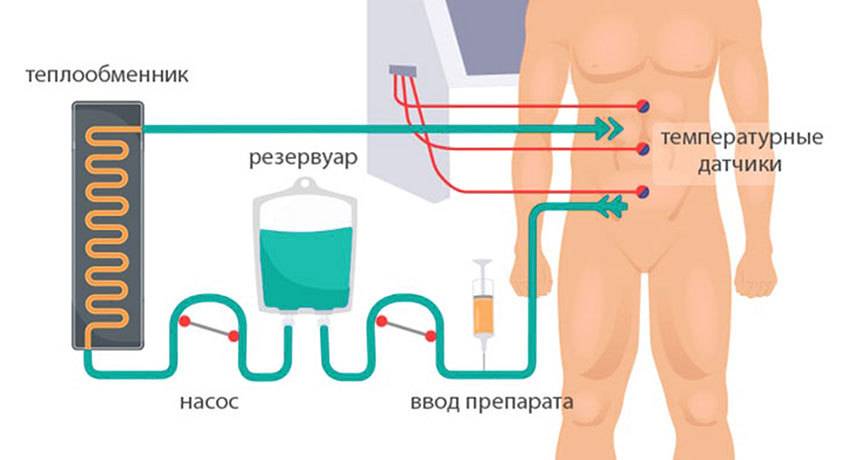 Схема проведения HIPEC
Схема проведения HIPEC
4) Реконструктивная операция. Если удалены части кишечника, хирург восстанавливает непрерывность кишки — формирует анастомоз, выводит верхний конец толстой/тонкой/слепой кишки на поверхность живота для отхождения каловых масс.
В среднем, в клинике пациент проводит 2–4 недели. Через 2–3 недели после операции проводится контрольное обследование. Его необходимо повторять через 3 месяца, и постепенно частоту проверок снижают до 1 раза в год.
В этом видео наши коллеги проводят процедуру HIPEC пациентке с раком яичников.
Причины лимфомы желудка
Причины развития лимфом желудка неизвестны, и не определены мутации генов, ведущие к перерождению нормальных клеток. В семейной истории страдавших лимфомами желудка часто имеются родственники со злокачественными заболеваниями.
В инициации опухоли предполагается соучастие нарушений иммунитета:
- избыточной защиты при аллергии и аутоиммунных болезнях;
- иммунодефицита при ВИЧ и наследственных синдромах;
- нарушений толерантности при противоопухолевой терапии и хроническом воспалении;
- угнетении из-за повышенного радиационного воздействия.
Определенная этиологическая роль принадлежит хеликобактерной инфекции, у большинства пациентов в желудочном секрете находят Helicobacter pylori (Н.pylori). Скопления В-лимфоцитов в желудочной стенке, из которых развивается опухоль, возникают при вызываемом и поддерживаемом бактериями хроническом воспалении. Выявление хеликобактерной инфекции и её лечение — основополагающий подход при MALT (мукозоассоциированном) варианте опухоли.
Методы лечения
Наиболее распространенные методы лечения лимфом:
- лучевая терапия;
- химиотерапия;
- радиотерапия;
- биологическая терапия;
- трансплантация стволовых клеток;
- хирургическое вмешательство.
Они применяются как в виде отдельных курсов, так и в комплексе. Выбор лечебной схемы зависит от вида опухоли и общего состояния больного.
Лечебная тактика
Индолентные лимфомы могут не требовать лечения, а только наблюдения онкогематолога. Терапия показана при первых признакахпрогрессированияпатпроцесса. При локализованныхопухоляхдостаточнорадиотерапевтического облучения пораженных структур. При генерализованных формах показана химиотерапия.
При агрессивном течении заболевания одна из наиболее эффективных лечебных схем – химиотерапия по протоколу СНОР в сочетании с иммунотерапевтическимипрепаратами из группы моноклональных антител. При высокоагрессивных видах опухолей может быть назначена высокодозная химиотерапия в сочетании с трансплантацией кроветорных стволовых клеток.
Лечение отдельных типов лимфом
Радиотерапия – излучение высокой мощности – в качестве самостоятельного лечения ЛГМ может быть оправдана в отдельных случаях – когда в процесс вовлечена одна, максимум две группы лимфатических узлов. Чаще ее назначают в комплексе с химиотерапией. На поздних стадиях заболевания метод показан в качестве паллиативного лечения.
Биологические препараты – моноклональные антитела – при лечении лимфомы применяют для активизации иммунной системы. Лучевую терапию проводят регионарно, в области вовлеченных в онкологический процесс лимфоузлов.
В некоторых случаях при лечении ЛГМ оправдано удаление селезенки. Если увеличенные лимфатические узлы сдавливают соседние органы,может быть показано их иссечение.
При рецидивах заболевания, а также с целью уничтожения раковых клеток, на которые не действуют стандартные дозировки лучевой и химиотерапии, назначают высокие терапевтические дозы, разрушающие вместе с опухолью ткани костного мозга. После такого курса показана трансплантация органа. Взятые заранее собственные либо донорские стволовые клетки формируют новую иммунную систему.
Хорошие результаты в лечении НХЛ демонстрирует также комбинация лучевой и химиотерапии. В некоторых случаях успешно применяют инновационную техникулюмбально-пункционного введения противоопухолевых антител.
НХЛ с агрессивным течением плохо поддаются лечению. Наиболее эффективный метод борьбы с этим заболеванием – пересадка костного мозга.
Этиология заболевания
Причины лимфаденопатии:
- Вирусные инфекции. В эту группу болезней входят краснуха, ветряная оспа и корь. Увеличенные лимфоузлы под мышкой могут быть симптомом цитомегаловируса, в то время как опоясывающий лишай, мононуклеоз или ВИЧ связаны с аналогичными изменениями в области уха и нижней челюсти.
- Бактериальные инфекции. Например: туберкулез, скарлатина, туляремия или стафилококковая инфекция.
- Грибковые поражения.
- Онкологические заболевания. При опухолевых заболеваниях лимфатические узлы могут увеличиваться в случае метастазов (вторичная форма), а также при онкологии самой лимфатической системы (лимфомы).
Появление лимфаденопатии может быть связано с аутоиммунными заболеваниями: системной красной волчанкой, болезнью Хашимото или ревматоидным артритом.
Причины гиперплазии лимфоузлов
Но нас интересуют именно регионарные лимфатические узлы, которые обеспечивают выработку лимфоцитов и антител, фильтрацию лимфы и регулирование ее токов из органов. На сегодняшний день причины гиперплазии лимфоузлов рассматриваются как причины их увеличения, которое является иммунным ответом на любой патологический процесс, вносящий изменения как в динамику тканевого метаболизма лимфатического узла, так и в соотношение тех или иных клеток. Например, при реакции на генетически отличные клетки (антигены) в лимфатическом узле повышается выработка лимфоцитов и мононуклеарных фагоцитов (макрофагов); при попадании бактерий и микробов в лимфоузлах скапливаются продукты их жизнедеятельности и обезвреженные токсины. А в случае онкологии гиперплазия лимфоузлов способна вовлечь в патологический процесс пролиферации любые их клетки. Это вызывает увеличение размера, изменение формы и структуры фиброзной капсулы лимфатического узла. Более того, ткани лимфатических узлов могут прорастать за пределы капсулы, а в случае метастазов из других органов вытесняться их злокачественными клетками.
Исходя из этого, гиперплазия лимфоузлов может быть инфекционного, реактивного или злокачественного происхождения.
[], [], [], [], [], [], [], [], [], []
Гиперплазия лимфоузлов инфекционной этиологии
Гиперплазия лимфоузлов (в смысле увеличение их размеров) является ответом на инфекцию при таких заболеваниях, как вызванный стрепто- или стафилококками лимфаденит, краснуха, ветряная оспа, инфекционный гепатит, фелиноз (болезнь кошачьей царапины); туберкулез, ВИЧ, инфекционный мононуклеоз, цитомегалия, туляремия, бруцеллез, хламидиоз, сифилис, актиномикоз, лептоспироз, токсоплазмоз.
При неспецифических лимфаденитах – в зависимости от локализации – наблюдается гиперплазия лимфоузлов в области шеи, нижней челюсти или подмышечных лимфатических узлов. Увеличение аксиллярных лимфоузлов отмечено при мастите, воспалениях суставов и мышечных тканей верхних конечностей, бруцеллезе, фелинозе и др.
Для воспалительных процессов в полости рта и носоглотки (при актиномикозе, кариесе, хроническом тонзиллите, фарингите, бронхите и др.) характерна гиперплазия подчелюстных лимфоузлов, заушных, предгортанных и заглоточных. А при инфекционном мононуклеозе увеличиваются только шейные лимфатические узлы.
В случае краснухи, токсоплазмоза, туберкулеза, а также при сифилисе врачи констатируют гиперплазию шейных лимфоузлов. Кроме того, в симптоматике туберкулеза отмечаются гиперплазия внутригрудных, а также лимфоузлов средостения. При этом в лимфатических узлах происходит постепенное вытеснение здоровых клеток лимфоидной ткани некротическими массами казеозного характера.
Свойственна туберкулезу и гиперплазия брыжеечных лимфоузлов. Кроме того, значительное увеличение лимфатических узлов брыжеечного отдела тонкой кишки происходит вследствие поражения грамотрицательной бактерией Francisella tularensis, которая вызывает туляремию – острое инфекционное заболевание, переносимое грызунами и членистоногими.
Стадии лимфомы
Лимфома является системным заболеванием. При прогрессировании она может поражать всю лимфатическую систему и даже выходить за ее пределы, распространяясь на внелимфатические органы и ткани.
Если на начальных стадиях при лимфоме средостения имеется поражение только медиастинальных лимфатических узлов, то по мере распространения, в процесс вовлекаются другие группы. В этой связи выделяют 4 стадии заболевания:
- 1 стадия — поражена одна лимфатическая зона, т. е. увеличены только медиастинальные лимфоузлы.
- 2 стадия — имеется поражение лимфоузлов двух зон по одну сторону диафрагмы, например, увеличены медиастинальные лимфоузлы и надключичные.
- 3 стадия — имеются единичные очаги поражения по обе стороны диафрагмы.
- 4 стадия — имеются множественные очаги поражения по обе стороны диафрагмы.
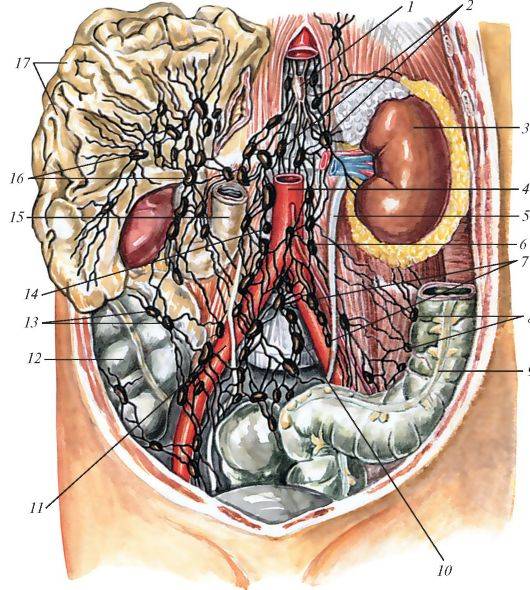
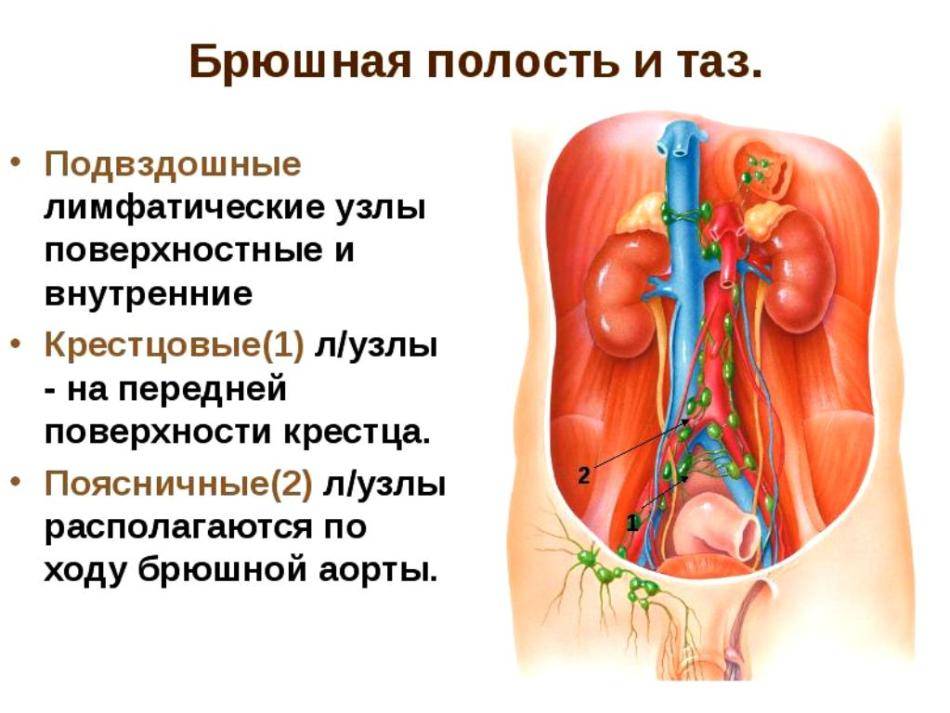
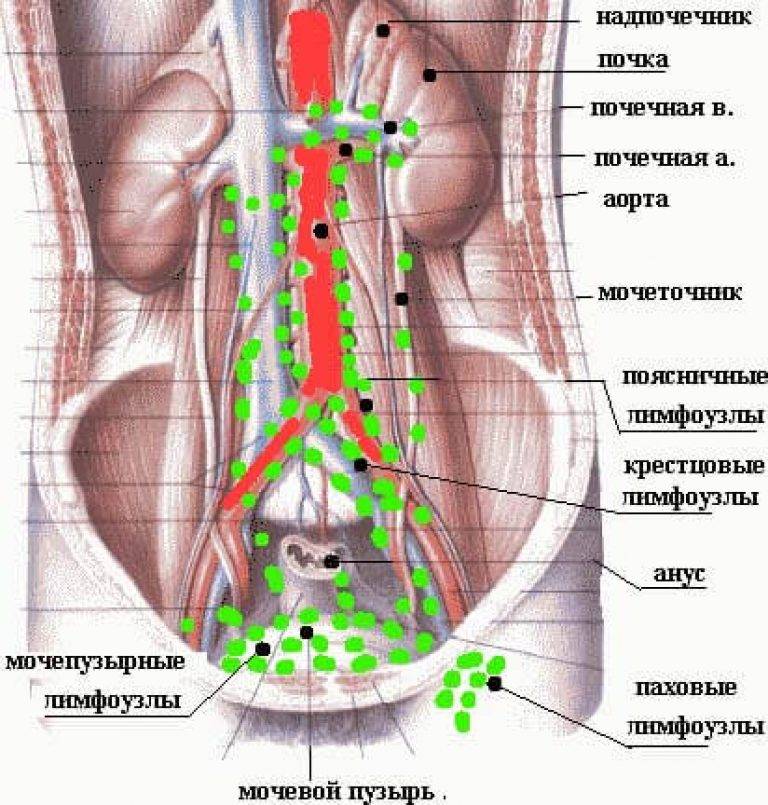
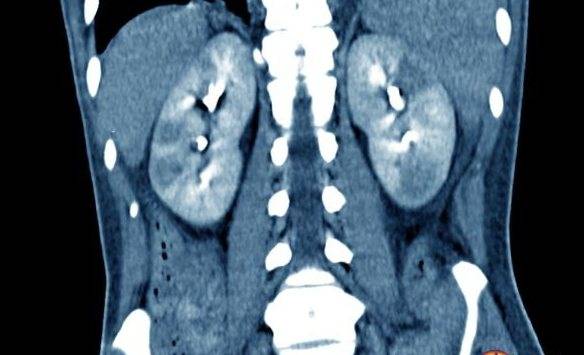
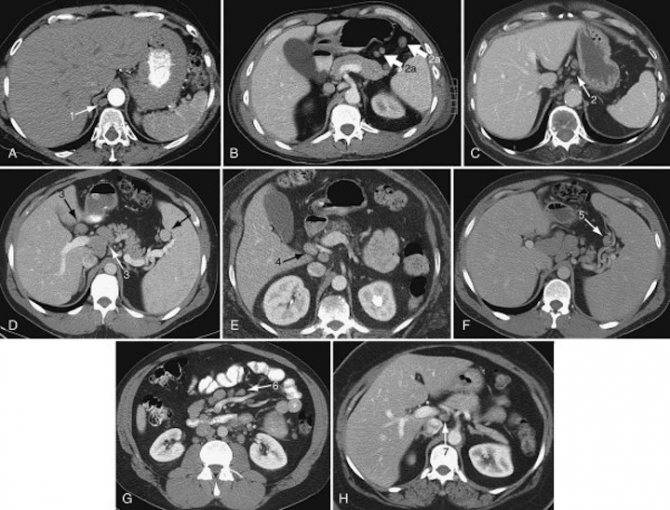
Метастазы в парааортальные лимфоузлы
Местоположение парааортальных лимфоузлов – передняя часть поясничного отдела позвоночника, вдоль аорты.
Метастазы в парааортальные лимфоузлы наблюдаются у пациентов с раком половой сферы, почек и надпочечников, отделов ЖКТ. Например, при злокачественных новообразованиях желудка в 40% случаев выявляются пораженные парааортальные лимфатические узлы. Опухолевые процессы с метастазированием в парааортальные лимфоузлы относят к третьей-четвертой стадии заболевания. Причем частота поражения парааортальных узлов третьей степени онкологии достигает 41%, а четвертой степени – 67%. Следует отметить, что например, метастазы в парааортальные лимфоузлы рака яичников имеют устойчивость к химиотерапии.
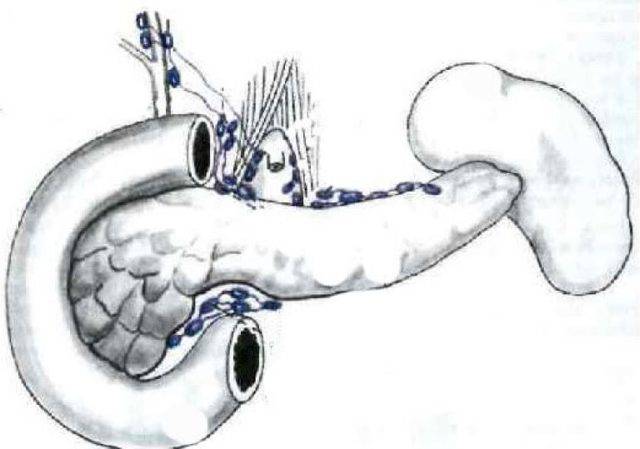
Развитие рака поджелудочной железы имеет свои этапы лимфогенного метастазирования:
- первая стадия – метастазы достигают головки поджелудочной;
- вторая стадия – поражаются ретропилорические и гепатодуоденальные лимфоузлы;
- третья стадия – проникновение метастаз в чревные и верхние брыжеечные узлы;
- четвертая стадия – метастазирование в парааортальные лимфоузлы.
Медики отмечают, что злокачественные опухоли поджелудочной железы характеризуется агрессивным течением и имеет плохой прогноз. Случаи летального исхода от рака поджелудочной занимают 4-5 место среди всех онкологических заболеваний. Высокая смертность связана с рецидивированием опухолевых процессов в послеоперационный период (К-ras мутации в парааортальные лимфоузлы).
Диагностика лимфомы желудка
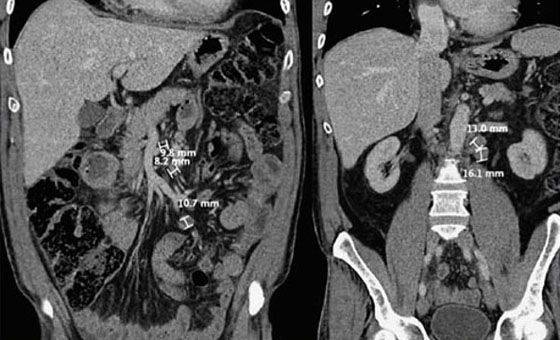
Диагностика лимфомы на первом этапе не отличается от выявления других злокачественных процессов желудка: эндоскопия с биопсией, УЗИ, КТ брюшной полости, КТ грудной клетки.
Как при всех злокачественных процессах крови и лимфатической ткани обязательно выполняется трепанобиопсия костного мозга.
После морфологической верификации проводится уточняющая терапию диагностика:
- тесты на выявление в желудочном содержимом Helicobacter Pylori;
- определяется чувствительность хеликобактера к антибиотикам;
- цитогенетический анализ на обнаружения переноса участка t(11;18) с одной хромосомы на другую, при выявлении транслокации проводится уточняющий FISH-анализ.

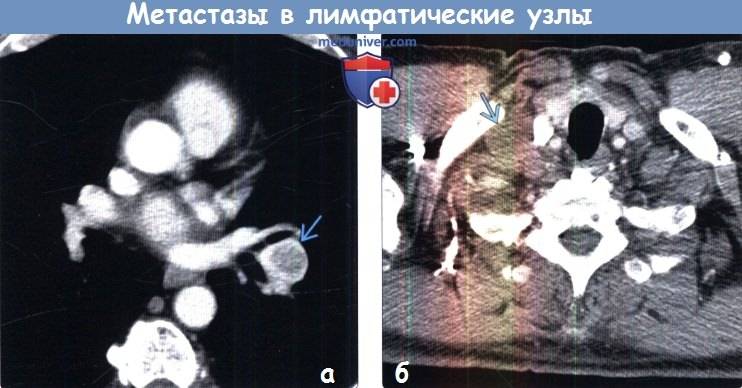
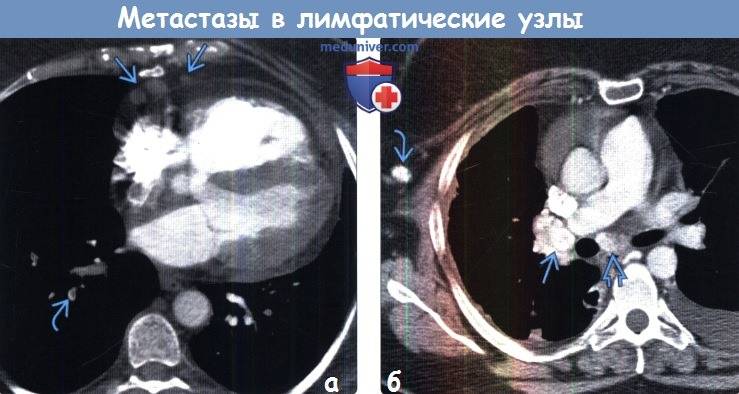
Метастазы в лимфоузлах средостения
Средостение – это отдел грудной полости, которую ограничивает спереди грудина, реберные хрящи и позагрудинная фасция, сзади – передняя зона грудного отдела позвоночника, шейки ребер, предпозвоночная фасция, по бокам – листки средостенной плевры. Область средостения снизу обозначена диафрагмой, а сверху – условной горизонтальной линией. В зону средостения попадают грудной лимфопроток, загрудинные лимфоузлы, передние лимфоузлы средостения.
Кроме рака легких метастазы в лимфоузлах средостения образовывают опухолевые процессы щитовидной железы и пищевода, гипернефрома почки, рак яичка (семинома), пигментное злокачественное образование (меланосаркома), рак матки (хорионэпителиома) и другие новообразования. Поражение лимфоузлов средостения занимает третье место в развитии злокачественных процессах после лимфогранулематоза и лимфосаркомы. Раковые клетки охватывают все группы лимфоузлов средостения, наиболее часто поражаются паратрахеальные и бифуркационные.
Первичные опухоли небольшого размера зачастую дают обширные метастазы в лимфоузлах средостения. Ярким примером подобного метастазирования является рак легкого медиастинальной формы. В клинической картине описывается отечность мягких тканей шеи и головы, набухание и переплетение вен спереди грудной клетки («голова медузы»), отмечается дисфагия, осиплость, дыхание стридорозного типа. Рентген в большинстве случаев выявляет преобладание метастаз в заднем средостении.
Диагностика увеличенных лимфоузлов
Самое главное при диагностике лимфаденопатии — определить ее причину.
Врач при пальпации оценивает размер, консистенцию, подвижность и болезненность лимфатических узлов. Одновременно оцениваются другие жалобы и общее состояние пациента, и на основании этих данных и данных обследования принимается решение о необходимости более глубокого обследования — анализа крови, рентгена, ультразвука и других исследований.
- Инфекционные заболевания характеризуются мягкими, болезненными, гибкими, увеличенными лимфатическими узлами.
- Лимфогранулематоз и метастазы опухоли характеризуются твердыми неподвижными лимфатическими узлами.
Возможно обследование непосредственно измененных лимфатических узлов. Выполняется их аспирация и микробиологическое исследование — содержимое лимфоузла отсасывается иглой и исследуется микробиологами.
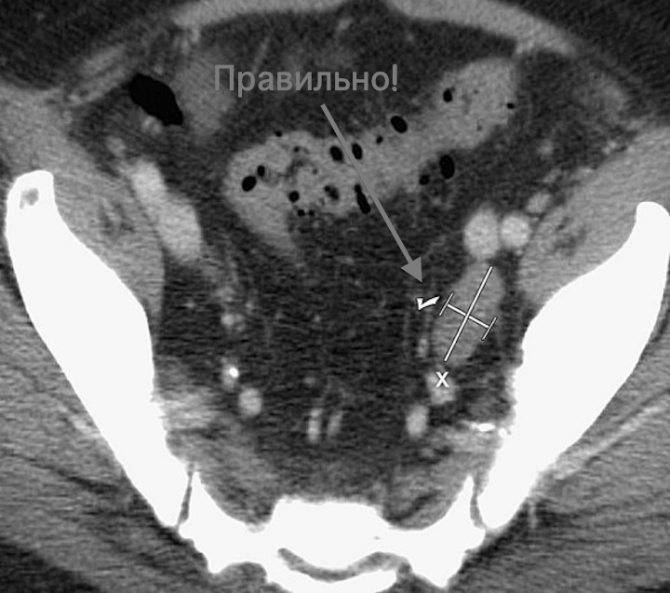
Может быть проведена биопсия лимфатического узла — процедура, при которой небольшой кусочек ткани берется с помощью специально подготовленной иглы и оцениваются изменения, наблюдаемые под микроскопом. Биопсия лимфатических узлов выполняется, если лимфатические узлы увеличены и причину их увеличения невозможно определить другими способами — подозрение на лимфому Ходжкина, метастазы рака, туберкулез, саркоидоз.
Биопсия лимфатического узла
Если в общем анализе крови обнаружены изменения, может потребоваться исследовать костный мозг.
В общем, если увеличенный лимфатический узел обнаружен только в одной области, пациента следует обследовать на предмет всех заболеваний и патологий, связанных с этой областью. При обнаружении большого количества увеличенных лимфатических узлов проводится комплексное обследование.
Стадии лимфом
В зависимости от распространенности опухоли определяют стадию патологического процесса. В соответствии с международной классификацией AnnArborвыделяют 4 стадии заболевания:
- На 1-й стадии в лимфомный процесс может быть вовлечена одна группа лимфатических узлов.
- На 2-й допускается вовлечение двух и более групп по одну сторону от диафрагмы.
- На 3-й стадии опускается поражение лимфатических узлов по обе стороны диафрагмы.
- На 4-й стадии в процесс вовлекаются внутренние органы – мозг, сердце, печень, селезенка, желудок, кишечник.
Каждую стадию дополнительно маркируют титрами А и Б. Титр А указывает на отсутствие ключевых симптомов – лихорадки, сильной ночной потливости и резкого снижения веса. Титр Б указывает, что такие проявления есть.
Виды и стадии лимфаденопатии
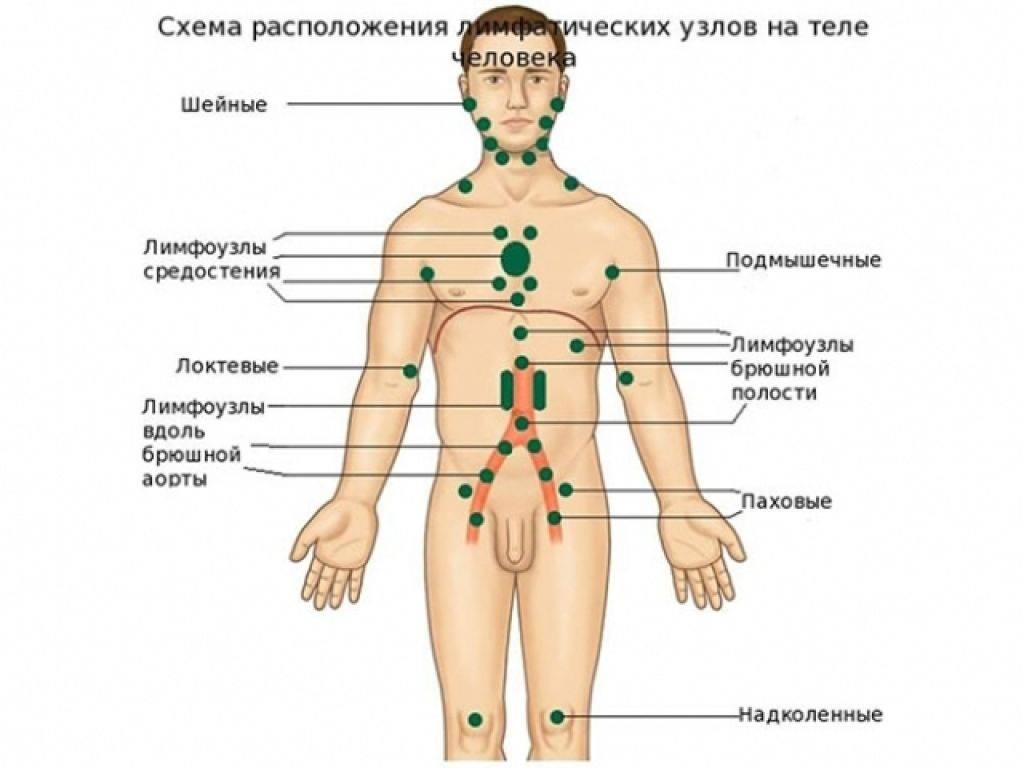
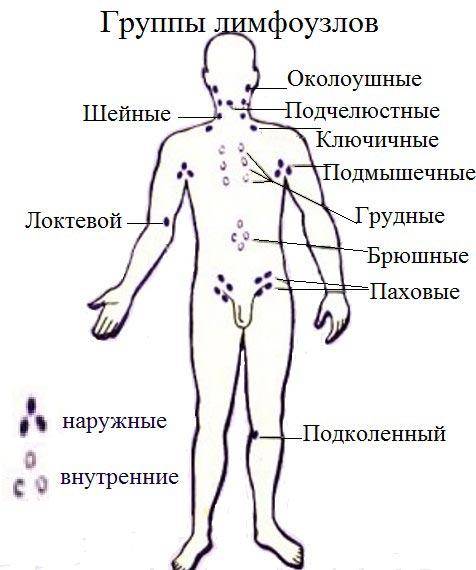
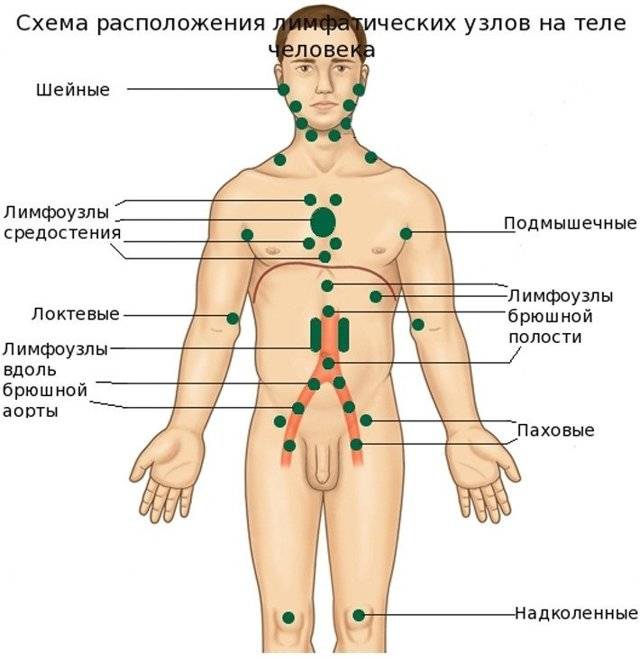
Условно лимфатические узлы делятся на периферические и внутренние лимфатические узлы:
- Периферические лимфатические узлы — это лимфатические узлы, к которым можно прикоснуться. Можно пальпировать лимфоузлы, расположенные сзади и спереди уха, лимфатические узлы миндалин (расположены в углу нижней челюсти), верхнечелюстные лимфатические узлы, подбородочные, шейные, поростикулярные, затылочные, подмышечные, паховые, лопаточные, а иногда и брюшные лимфатические узлы.
- Внутренние лимфатические узлы — это лимфатические узлы внутри тела — внутренние (внутригрудные), преаортальные (парааортальные), соединительные (брыжеечные) и другие.
Симптомы воспаления лимфатических узлов
Воспаление регионарного подмышечного лимфоколлектора сопровождает все инфекционные процессы молочной железы, в первую очередь, лактационный мастит и гнойные кожные инфекции: фурункул, карбункул, абсцесс. В подмышечной области определяется умеренно увеличенный, но весьма болезненный лимфатический узел или несколько узлов, при далеко зашедшем воспалении может образоваться гной, который прорвётся наружу.
Нередко при инфекции на первый план выходят симптомы лимфаденопатии, тогда как в самой молочной железе нет явных воспалительных проявлений. Лимфаденопатия может развиться через неделю-две после полного заживления процесса в тканях груди.
Диагностика
При диагностике врач должен дифференцировать острый панкреатит от аппендицита, холецистита, прободной язвы желудка, острой кишечной непроходимости, острого ишемического абдоминального синдрома и других острых состояний с похожими симптомами.
В клинике «Медицина 24/7» проводится полный комплекс диагностических обследований при остром воспалении поджелудочной железы.
- Общее и биохимическое исследование крови. Общий и биохимический анализы крови при остром панкреатите показывают повышение уровня лейкоцитов, СОЭ, пониженный гематокрит (объем кровяных телец), повышение уровня амилазы, липазы, глюкозы, снижение уровня общего белка, альбуминов, глобулинов, повышение уровня С-реактивного белка, мочевины.
- Биохимический анализ мочи. Исследование мочи показывает повышение уровня амилазы, наличие эритроцитов, лейкоцитов, белков.
- Ионограмма. Это исследование показывает снижение уровней кальция, натрия, калия в крови в результате неукротимой рвоты и обезвоживания организма.
- УЗИ поджелудочной железы и органов брюшной полости. Ультразвуковое исследование показывает увеличение поджелудочной железы, участки неоднородности ее ткани, изменение формы, неровность ее контуров, наличие жидкости в брюшной полости, забрюшинном пространстве.
- Рентген. Рентгенография живота и нижней части легких показывает вздутие кишечника, наличие плеврального выпота.
- Лапароскопия. Это визуальный метод обследования. Через прокол в брюшной стенке внутрь вводится миниатюрная видеокамера с подсветкой, изображение с которой поступает на монитор компьютера. С его помощью врач может установить причину закупорки протока поджелудочной железы, исследовать очаг воспаления, обнаружить геморрагический экссудат, участки некроза ткани, кровоизлияния и другие характерные признаки заболевания.
- КТ. Компьютерная томография помогает обнаружить участки некроза ткани поджелудочной железы, псевдокисты, подробно исследовать структуру органа.
- МРТ. Магнитно-резонансная томография может быть использована для получения дополнительных диагностических данных.
Осложненные формы
При отсутствии быстрой медицинской помощи острый панкреатит может дать множество осложнений, в том числе тяжелых, угрожающих жизни человека.
Вот почему при симптомах острого воспаления требуется быстрая госпитализация больного в хирургическое отделение или в отделение реанимации и интенсивной терапии.
Клиника «Медицина 24/7» осуществляет срочную транспортировку больных с немедленным оказанием первой медицинской помощи.
Осложненные формы острого панкреатита бывают связаны с двумя факторами — попаданием ферментов поджелудочной железы в кровь и присоединением инфекции.
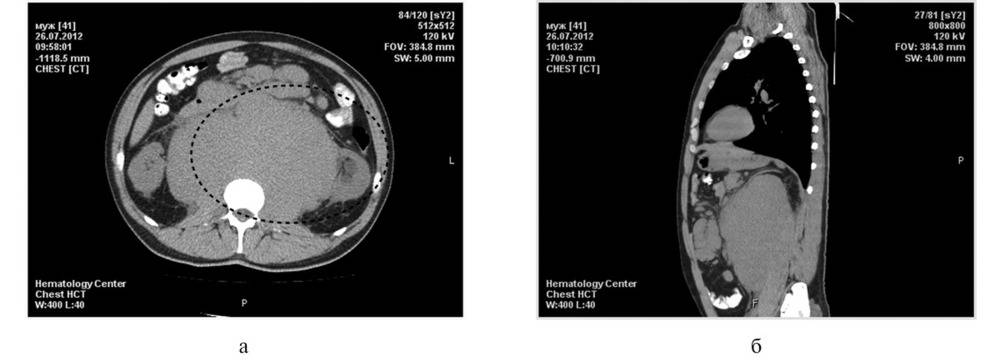
Наиболее частые осложнения, при которых проводится хирургическое лечение — образование участков некроза тканей, скопление воспалительной жидкости (экссудата), гнойное воспаление (абсцесс), перитонит.
Жидкость может скапливаться как внутри самой поджелудочной железы, так и вокруг нее, образуя асцит — водянку.
- Полиорганная недостаточность.Из-за острого воспаления, попадания панкреатических ферментов в кровь и токсического воздействия развивается полиорганная недостаточность.
- Дыхательная недостаточность.На фоне острого воспаления поджелудочной железы возможно развитие синдрома, который называется «шоковым легким» — быстрое развитие экссудативного плеврита, дыхательной недостаточности, спадение легкого.
- Почечная, печеночная недостаточность.Эти осложнения развиваются из-за токсического воздействия ферментов, попавших в кровь.
- Сердечно-сосудистая недостаточность.Поражение сердца при остром панкреатите имеет общую причину с развитием почечной, печеночной недостаточности — токсическое действие ферментов, попавших в кровь.
- Перитонит.Одно из частых осложнений, которые дает острый панкреатит — воспаление брюшной полости, которое бывает гнойным (инфекционным) или асептическим (без инфекции).
- Расстройства психики.Токсическое воздействие панкреатических ферментов на мозг вызывает изменение психоэмоционального состояния вплоть до развития психоза.
- Сепсис.Развитие гнойного процесса на фоне острого панкреатита может вызвать заражение крови (сепсис), которое требует экстренных мер. В противном случае сепсис может привести к смерти.
- Абсцессы.Присоединение инфекции вызывает образование гнойников в брюшной полости.
- Парапанкреатит.Гнойное воспаление может распространиться на окружающие органы — сальник, забрюшинную клетчатку, брюшину, связки печени, 12-перстной кишки.
- Псевдокисты.Вокруг некротических очагов в поджелудочной железе могут образоваться капсулы из соединительной ткани — так возникают псевдокисты, наполненные жидкостью или гноем.
- Опухоли.Острое воспаление может спровоцировать перерождение клеток и развитие онкологического заболевания поджелудочной железы.
Реактивная гиперплазия лимфоузла
Реактивная гиперплазия лимфоузлов возникает как ответная реакция иммунной системы на патологии иммунного же характера. К таким патологиям относятся:
- аутоиммунные коллагенозы (ревматоидный артрит и полиартрит, узелковый периартериит, системная красная волчанка, склеродермия, синдром Хаммена-Рича, грануломатоз Вегенера); – болезнь Вагнера или дерматомиозит (системное заболевание скелетной и гладкой мускулатуры и кожи)
- болезни накопления (эозинофильная гранулема, болезнь Гоше, болезнь Ниманна-Пика, болезнь Летерера-Зиве, болезнь Хенда-Шюллера-Крисчена).
Помимо этого, реактивная форма может сопутствовать сывороточной болезни (аллергии на применение иммунных сывороточных препаратов животного происхождения), гемолитическим анемиям (наследственным или приобретенным), мегалобластной анемии или болезни Аддисона-Бирмера (которая возникает при дефиците витаминов В9 и В12) и химиотерапии и лучевой терапии онкологических заболеваний.
Среди аутоиммунных заболеваний эндокринной системы гиперплазия лимфоузла характерна для гипертиреоза (Базедовой болезни), причина которой кроется в повышенной выработке щитовидной железой тиреоидных гормонов. При этой патологии гиперплазия лимфатических узлов носит генерализованный характер с повышенным митозом лимфатических фолликулов.
Специалисты подчеркивают, что реактивная гиперплазия лимфоузла отличается значительной пролиферативной активностью и, как правило, затрагивает лимфатические узлы в области шеи и нижней челюсти.
С точки зрения цитоморфологии, реактивная форма имеет три вида, самым распространенными из которых является фолликулярная форма.
Симптомы опухолевой лимфаденопатии
Поскольку подмышечные лимфоузлы ближайшие к молочной железе, при наличии новообразования в железе высока вероятность появления и развития в них раковых клеток. Это происходит настолько часто, что в классификации рака молочной железы они не учитываются как метастазы — символ М, хотя формально это метастазирование.
С одной стороны, на раннем этапе рака подмышечный лимфатический коллектор защищает от дальнейшего распространения клеток по организму, но при формировании опухоли уже в самом узле он становится самостоятельным источником болезни.При раковом поражении в подмышке определяется от одного увеличенного лимфоузла до бугристого конгломерата спаянных между собой нескольких крупных узлов. Боли возникают при значительном увеличении опухоли и сдавлении ею нервных стволов, проходящих в подмышечной области.
Диагностика рака лимфоузлов
В рамках диагностики рака лимфатической системы требуется комплексный подход, который направлен на подтверждение диагноза и на определение его стадии.
Диагноз выставляется только после патоморфологического исследования фрагмента пораженного лимфоузла. С этой целью необходимо произвести биопсию. Полученный материал заливают парафином и делают из него препараты, нарезая опухоль тонким слоем, чтобы ее можно было исследовать под микроскопом. Также применяют дополнительные лабораторные методы диагностики, например, иммуногистохимическое окрашивание, молекулярно-генетические тесты и др.
Для определения стадии заболевания используют лучевые методы диагностики:
- ПЭТ-КТ.
- КТ.
- МРТ.
- УЗИ.
- Сцинтиграфию.
С их помощью визуализируют пораженные лимфоузлы и внелимфатические очаги.
Когда при увеличении лимфоузлов надо бить тревогу?
— Если увеличение лимфоузлов сопровождается повышением температуры тела, необходимо обращаться к участковому врачу. Врач на приеме часто исследует доступные для осмотра группы лимфоузлов, так как при воспалительных заболеваниях отмечается их болезненность. При воспалении лимфоузла во время прогрессирования инфекционного процесса могут возникать следующие патологические признаки:
- покраснение, отечность лица и шеи;
- боль при пальпации увеличенного узла;
- выраженный озноб;
- слабость, признаки интоксикации, ломота в мышцах, головная боль, снижение работоспособности;
- повышение температуры тела.
При сниженном иммунитете и неэффективности проводимой терапии порой может развиваться опасное для больного осложнение — флегмона, которая может закончиться сепсисом.
Кроме того, пристального внимания требуют так называемые немые лимфоузлы, появившиеся без температурной реакции, безболезненные, плотные, чаще связанные с окружающими тканями и имеющие стойкую тенденцию к увеличению. Они зачастую причиняют дискомфорт (например, в подмышечной области) или приводят к отеку конечности. В таких ситуациях необходимо обращаться к участковому врачу, который после осмотра назначит общий анализ крови, флюорографию грудной клетки, осмотр хирурга для решения вопроса о пункции лимфоузла или направит к онкологу или фтизиатру.